食物反応(アレルギー、不耐症、感受性)
Posted by リンクプロ on
食物反応の定義
概要と要点
食物やその成分に対する反応にはいくつかの種類があります。
-
食物アレルギーは免疫系が関与する反応です(例:免疫グロブリンE(IgE)またはT細胞による反応)。
-
食物不耐症は免疫が関与しない反応です(例:酵素欠乏によるもの)。
-
食物過敏症は、アレルギーや食物不耐症として明確に分類されない有害反応を指します。一部の代替医療の専門家は、IgG抗体が食物過敏症に関与していると考えています。また、「食物過敏症」という用語は、非アレルギー性の食物反応を指す包括的な用語として使用されることがあります。
-
IgE媒介型の食物アレルギーは命に関わる可能性があるため、疑いがある場合は直ちにアレルギー専門医の診察を受ける必要があります。
-
腸内細菌叢の不均衡、腸の機能不全、一部の薬剤、遺伝的要因が寄与要因となることがあります。
-
一部の食物反応の症状を緩和し、全体的な健康を改善するために、特定の食事や生活習慣の変更が有効です。
-
ビタミンD、フラボノイド、プロバイオティクス、亜鉛、消化酵素などの栄養補助食品は、一部の食物反応の症状を緩和する助けとなる場合があります。
有害な食物反応とは、特定の食物やその成分を摂取したことによって引き起こされる症状を指します。これらの反応は軽度から重度までさまざまで、以下のような形で現れることがあります:
- 消化器の問題(例:膨満感、ガス、下痢、便秘、腹痛)
- 皮膚の発疹(例:じんましん、湿疹、乾癬、ニキビ)
- 頭痛や片頭痛
- 疲労感や倦怠感
- 関節の痛みやこわばり
- 集中力の低下や「脳の霧」
- 気分の変化(例:不安、抑うつ、いらだち)
- 呼吸器の問題(例:喘鳴、咳、鼻づまり)
- 不眠やその他の睡眠障害
- 筋肉の痛みや脱力感
- アナフィラキシー(重篤で命に関わる全身性アレルギー反応)
多くの人々は、特定の食物を摂取した後に不快感や有害な症状を経験すると、食物アレルギーがあると考えます。しかし、これらの症状はさまざまな種類の食物反応によって引き起こされる可能性があり、それぞれの反応は体が特定の食物または成分にどのように反応するかによって定義されます。一部の反応は即時で重篤なものもあれば、より微妙で遅延性のものもあります。
科学文献や一般メディアでは、食物やその成分に対する反応に関する用語が一貫していないことが多いです。この混乱を最小限に抑えるために、以下の定義を一貫して使用します。
食物反応の分類
-
食物アレルギー
食物アレルギーは、免疫系が関与し、再現性のある食物に対する有害反応です。これらは命に関わる場合があります。一般的な「食物アレルギー」の概念は、IgE(免疫グロブリンE)による急速な反応を指しますが、他の種類のアレルギー反応も存在します。 -
食物不耐症
食物不耐症は、免疫反応を伴わない消化器系の有害反応であり、再現性があります。これらは、特定の食物成分を消化するのが困難であることが原因と考えられます。例として、乳糖不耐症、ヒスタミン不耐症、発酵性オリゴ糖、二糖類、単糖類、ポリオール(FODMAPs)への反応などがあります。 -
食物過敏症
「食物過敏症」は、免疫媒介型の「アレルギー」や非免疫媒介型の「不耐症」とは異なる食物反応を指します。一部の革新的な医療従事者は、IgG抗体が時に食物過敏症に関与していると考えています。また、この用語は、非アレルギー性の食物反応を指す包括的な意味で使用されることもあります。 -
セリアック病
セリアック病は、グルテン中のタンパク質「グリアジン」によって引き起こされる自己免疫反応です。この反応は、パンが柔らかい食感を持つ理由であるグルテンに関連しています。一部の人々はグルテンにアレルギーを持つ場合がありますが、セリアック病はアレルギーには分類されません。セリアック病では、グルテンを摂取すると腸壁が誤って攻撃されます。
これらの分類に基づき、食物反応の種類や影響を適切に理解し、適切な対策を講じることが可能です。
原因と要因
食物アレルギー
食物アレルギーは以下のように分類されます5 :
- IgE媒介アレルギーは過敏症とも呼ばれ、ヒスタミン、ロイコトリエン、サイトカインなどの炎症因子の大量放出を引き起こします。
- 非IgE媒介性食物アレルギーでは、免疫系のT細胞がIgE媒介性以外のシグナルに反応して炎症性化学物質を放出します。
- IgE介在性アレルギーと非IgE介在性アレルギーの両方の特徴を持つ 混合型食物アレルギー
これらのアレルギーの主な違いは、アレルゲンに反応する免疫システムの部分と、反応のタイミングです。6米国の成人における食物アレルギーの有病率は約 3.5% から 10% の範囲と推定されています。3,7
IgE 介在性食物アレルギー。IgE介在性食物アレルギーは、一般的には真のアレルギーまたは典型的なアレルギーと考えられています。IgE 介在性食物アレルギーの症状は、免疫系が誤って食物成分 (多くの場合はタンパク質) を有害物質と認識し、食物アレルゲンに特異的な IgE 抗体を生成することで発生します。このアレルゲンへの最初の曝露は「感作」と呼ばれます。食物を再び摂取すると、IgE 抗体がアレルゲンを認識し、肥満細胞、好酸球、好塩基球と呼ばれる免疫細胞に信号を送ります。肥満細胞と好酸球は、脱顆粒と呼ばれるプロセスでヒスタミンやその他の化合物を放出します。これらの免疫メディエーター化合物の放出により、腫れ、かゆみ、うっ血、炎症などの問題のある厄介な症状が発生します。これらの反応は軽度である場合もありますが、アナフィラキシーショックの場合のように生命を脅かすこともあり、その場合は直ちに医師の診察が必要です。5-8 IgE 媒介食物アレルギーが疑われる場合は、生命を脅かす反応を避けるために、できるだけ早くアレルギー専門医による検査と指導を受ける必要があります。
感受性の高い人にIgE介在性アレルギーを引き起こす可能性のある一般的な食品には以下のものがあります8:
- ピーナッツ
- 木の実
- 牛乳(乳糖不耐症とは異なります)
- 卵
- 大豆
- 小麦(グルテン不耐症やセリアック病とは異なります)
- 魚
- 貝
- ゴマ
- 赤肉(ダニに刺されてアルファガルと呼ばれる化合物に過敏になることで起こる)
実際、上記のアレルゲンの一部に対する潜在的に重篤なアレルギーは非常に一般的であるため、米国食品医薬品局 (FDA) は、牛乳、卵、魚、甲殻類、木の実、ピーナッツ、小麦、大豆、ゴマなどのアレルゲンを含む製品には、製品ラベルにその旨を記載することを義務付けています。
アレルギーがなぜ発症するかについては多くの仮説があります。例えば、アレルギーは寄生虫やその他の有害な侵入者から体を守るための誤った免疫反応であるという説があります。しかし、寄生虫の脅威がそれほど大きくない先進国では、この同じ免疫反応がアレルギーの発症につながり、害を及ぼす可能性があります。9
-
経口耐性の喪失。自然に生じる経口耐性の喪失は、食物アレルギーのもう 1 つの要因であると思われます。10食物中の抗原に対する自然な反応は免疫耐性ですが、時間の経過とともに徐々に耐性が低下する人もいます。この問題により、特定の食物抗原に対する感作が起こり、IgE を介した食物アレルギーにつながります。11
経口免疫療法は、経口耐性の喪失を回避するために推奨される場合があります。経口免疫療法では、食物アレルギーのある人に経口摂取によって食物タンパク質を投与し、特定の食物アレルゲンに対する反応閾値を高めます。最初の投与量は非常に低く、その後、安全性を確保するために資格のあるアレルギー専門医の監督下で慎重に増やしていきます。このプロセスにより、脱感作が促進され、多くの人の経口耐性が徐々に回復します。10維持投与量は脱感作の持続に役立ちますが、標準化された維持投与量とスケジュールは、2024 年半ばの時点でまだ確立されていません。経口耐性の回復を目的とした経口免疫療法の安全性と有効性を判断するための研究が進行中です。経口免疫療法は、資格のある医療提供者の監督なしに試みるべきではありません。
腸内細菌叢は、免疫調節、短鎖脂肪酸(SCFA)の生成、粘膜バリアの完全性の維持などのメカニズムを通じて、食物アレルゲンに対する経口耐性を確立し維持する上で重要な役割を果たします。腸内細菌叢の不均衡(ディスバイオーシス)は食物アレルギーに対する感受性の増加と関連しており、プロバイオティクスとプレバイオティクスは治療効果をもたらす可能性があります。現在進行中の研究により、腸内細菌叢と食物抗原に対する免疫反応との複雑な関係が解明され続けています。12-14
- アレルゲンの交差反応。ある抗原に対して体内で生成される IgE 抗体は、「交差反応」と呼ばれるプロセスを通じて、他のタンパク質も認識することがあります。たとえば、カシューナッツのタンパク質は、ピスタチオなどの関連ナッツと構造的に類似しており、アレルギー反応を引き起こす可能性があります。花粉食物アレルギー症候群 (PFAS または PFS) としても知られる口腔アレルギー症候群では、植物の花粉に対して生成された IgE 抗体が、生の果物、野菜、ナッツのタンパク質と交差反応し、食べた直後に口、唇、顔、舌、喉のかゆみや腫れを引き起こします。ただし、IgE 抗体が認識する食品中のアレルゲンは、熱に敏感な (熱に不安定な) タンパク質であることが多いため、調理した果物や野菜は通常、反応を引き起こしません。8
非 IgE 介在性食物アレルギー。非 IgE 介在性食物アレルギーは、体の免疫系が食物中の特定のタンパク質を有害物質であるかのように反応し、炎症反応を引き起こすことで発生します。アレルゲンに結合して反応を引き起こす IgE 抗体の生成を伴う IgE 介在性食物アレルギーとは異なり、非 IgE 介在性反応には T 細胞と呼ばれる異なるタイプの免疫細胞が関与します。15,16これらの T 細胞はアレルゲンによって活性化され、炎症やさまざまな症状を引き起こすさまざまな免疫シグナル分子を放出します。非 IgE 介在性反応は通常、生命を脅かすものではありませんが、それでも重大な不快感や健康上の問題を引き起こす可能性があります。17一般的な非 IgE 介在性食物アレルギーは、乳児や幼児に影響を与えることが多いです。これらには、食物タンパク質誘発性腸炎症候群 (FPIES)、食物タンパク質誘発性腸症 (FPE)、食物タンパク質誘発性アレルギー性直腸結腸炎 (FPIAP) が含まれます。セリアック病は、成人と子供に発症する免疫介在性 (非 IgE) 食物反応です。3
混合型食物アレルギー。混合型食物アレルギーは、IgE 介在性免疫反応と T 細胞介在性免疫反応の両方が関与します。18症状 には、じんましん、腫れ、かゆみ、アナフィラキシー、嘔吐、下痢、腹痛、湿疹などがあります。食物アレルギーが IgE 介在性免疫反応と非 IgE 介在性免疫反応の両方を伴う場合、反応のタイミングが遅れる可能性があるため、診断と管理がより困難になる可能性があります。19さらに、具体的な症状はさまざまであることが多く、すぐに明らかになるとは限りません。混合型食物アレルギーの一般的な誘因には、牛乳、ピーナッツ、卵、甲殻類、小麦などがあります。18
-
好酸球性胃腸障害。好酸球性胃腸障害 (EGID) は、胃腸管における白血球の一種である好酸球の異常な蓄積を特徴とする慢性消化器疾患のグループです。これらの症状は、食道から直腸まで、胃腸管のどの部分でも発生する可能性があります。EGID の例には、好酸球性食道炎 (EoE)、アレルギー性好酸球性胃腸炎、好酸球性大腸炎、好酸球性腸炎などがあります。EGID の中では、EoE が圧倒的に多く見られます。EoE は乳児期に診断されることが多いですが、成人の診断率も増加しています。6、20、21
EGID の症状には、嘔吐、胃腸の痛み、嚥下困難、下痢、食欲不振、制酸剤に反応しない胃酸逆流などがあります。8,22時間の経過とともに、EGID が引き起こす炎症と損傷により、胃腸組織が肥厚し、胃腸系で食物が移動しにくくなる可能性があります。20
食物不耐性
免疫介在性食物アレルギーとは対照的に、食物不耐症は、消化器系が、ほとんどの人が通常許容できる量の特定の食品または食品成分を処理するのに苦労するときに発生します。23食物不耐症は免疫反応の結果ではなく、異常な消化反応を伴います。摂取した食品の量は症状の重症度に直接関連しており、アレルギー反応はごく少量のアレルゲンでも引き起こされる可能性があり、特定の食品または食品成分は、摂取するたびに同じタイプの症状を引き起こします。8,24食物不耐症の発生は、腸内での食物の吸収と分解を促進する特定の消化酵素の不足が原因である可能性があります。23典型的な例は、ラクターゼ酵素の欠乏による乳糖不耐症です。食物不耐症の典型的な症状は、多くの場合、膨満感、ガス、下痢、腹痛として現れます。6,25
炭水化物不耐症。特定の炭水化物が適切に消化吸収されない場合、浸透圧効果が生じ、小腸に水分が蓄積します。これにより膨満感が生じ、食物と水分が結腸に流れ込み、そこで細菌が炭水化物を発酵し、ガス(二酸化炭素、水素、メタンなど)が過剰に生成され、鼓腸や腸の痛みの原因となります。このような発酵しやすい炭水化物は、発酵性、オリゴ糖、二糖類、単糖類、ポリオールの頭文字をとって FODMAP と呼ばれます。23,25
消化器症状(下痢など)は、吸収不良炭水化物が細菌発酵を上回る速度で蓄積し、結腸に過負荷がかかり、消化不良を引き起こすなど、特定の条件下でのみ発生します。また、細菌発酵の効率は、特定の薬剤(抗生物質など)や炎症性疾患の存在によっても妨げられます。これらの状況がなければ、吸収不良炭水化物が少量でも不耐性の症状は引き起こされない可能性があります。
- 乳糖不耐症。 乳糖不耐症は、牛乳やその他の乳製品に含まれる糖の一種である乳糖を体が消化できない場合に起こる、食物に対する一般的な有害反応です。26-28これは、小腸で乳糖を分解する酵素であるラクターゼが体内で十分に生成されない場合に起こります。症状は一般に摂取量に比例します(つまり、乳製品を多く摂取するほど、症状が悪化する可能性があります)。米国における乳糖不耐症の有病率は人口の約 36% です。ただし、有病率は世界中で大幅に異なり、ヨーロッパの多くの地域では有病率が低く(一般に 10~40%)、中東(約 50~90%)と中央アフリカ(約 80~100%)では有病率がはるかに高くなります。29,30 乳糖不耐症の最も一般的な治療法は、乳製品を避け、ラクターゼ酵素を補給することです。
- フルクトース不耐症。フルクトース不耐症は、多くの果物、野菜、蜂蜜や高フルクトースコーンシロップなどの甘味料に含まれる糖の一種であるフルクトースを含む食品に対する有害反応です。この症状は、おそらくフルクトーストランスポーターの欠乏により、体が小腸でフルクトースを効率的に吸収できない場合に発生します。このため、フルクトース不耐症は、症状がフルクトースを分解するのではなく輸送できないことによって引き起こされるため、通常、フルクトース吸収不良と呼ばれます。25酵素アルドラーゼBの遺伝性変異もフルクトース過敏症を引き起こす可能性がありますが、これはまれです。31フルクトース不耐症は通常、呼気検査によって診断されます。キシロースイソメラーゼなどの酵素の補給はフルクトース不耐症の治療に使用される場合がありますが、症状を 最小限に抑えるためにフルクトースを含む食品を避けることでこの状態を管理します。31,32果糖の濃度が高い食品には、蜂蜜、ドライフルーツ、フルーツジュース、アガベシロップや高果糖コーンシロップなどの甘味料、バーベキューソースや一部のサラダドレッシングなどの甘いソース、梨、イチジク、マンゴーなどの果物が含まれます。33
- スクロース不耐症。先天性のスクラーゼ-イソマルターゼ欠損症はスクロース不耐症を引き起こします。スクロースは、さまざまな果物、野菜、ナッツに含まれる天然の糖で、テーブルシュガーもスクロースです。また、デンプンの消化中に放出される炭水化物であるイソマルトースに対して、軽度の否定的な反応を示す人もいます。25スクロース不耐症は十二指腸生検で診断されます。34多くの食品にこれらの炭水化物が含まれているため、サクロシダーゼ(スクラーゼ)酵素サプリメント(スクライド)の摂取が必要になることがよくあります。35,36成人におけるスクロース不耐症の有病率の推定値は、地域、民族、研究間、診断方法によって異なります。ある研究では、水素メタン呼気試験では約 34%、13C-スクロース呼気試験では約 27% のスクロース吸収不良の発生率が報告されています。34別の研究では、蔗糖不耐症を引き起こすスクラーゼイソマルターゼ欠損症の発生率は、北米では 0.2%、グリーンランドのイヌイットでは 10.0% の範囲にあることが示されています。これらのばらつきは、成人人口における蔗糖不耐症の複雑さと潜在的な診断不足を浮き彫りにしています。37
薬理学的または化学的食物不耐症。薬理学的または化学的食物不耐症は、体に影響を及ぼす食品に含まれる添加物や天然化学物質(他のほとんどのタイプの反応の場合のようにタンパク質ではなく)の存在により、特定の食品に対して人が有害反応を経験するときに発生します。6,38薬理学的食物不耐症の症状を引き起こす可能性のある化学物質には、カフェイン、ヒスタミン、その他の生体アミンなどがあり、これらは通常、アミノ酸(つまり、タンパク質の構成要素)が酵素によって分解されるときに生成される特定のタイプの分子です。
- カフェイン。カフェインは、コーヒー、紅茶、エナジードリンク、チョコレートなどの食品や飲料に含まれる一般的な刺激物です。しかし、カフェインを特に大量に摂取すると、頭痛、睡眠障害、神経過敏などの悪影響が出る人もいます。カフェイン不耐性は、カフェインを効果的に代謝または処理できないこと、または過剰に摂取することで引き起こされ、これらの副作用を引き起こします。カフェインは肝臓でシトクロム P450 酵素と呼ばれる酵素群によって分解されますが、これらの酵素の活性に影響を与える遺伝的変異により、カフェイン代謝が遅くなったり速くなったりすることがあります。カフェイン代謝の速度は、カフェイン関連の副作用のリスクに影響します。代謝が遅い人は、カフェイン不耐性を経験する可能性が高くなります。39 23andMe が提供するような遺伝子検査では、CYP1A2 と呼ばれる遺伝子変異が肝臓がカフェインを代謝する速度の指標となるため、カフェイン代謝状態に関するレポートが提供されます。40スタチン、抗うつ薬、抗てんかん薬などの特定の薬剤もこれらの酵素を誘導または阻害し、重大な薬物相互作用やカフェインに対する予期しない副作用を引き起こす可能性があります。41,42
- ヒスタミンと生体アミン。ヒスタミンはアレルギー反応や炎症反応の信号として働く化学伝達物質です。43しかし、多くの食品にヒスタミンが含まれています。ヒスタミン不耐症は、ジアミンオキシダーゼ (DAO; 摂取したヒスタミンを分解する腸内の酵素) の欠乏または食事中のヒスタミン過剰により、体がヒスタミンを効率的に分解できない場合に発生します。44,45 DAOレベルまたは活性の低下は、遺伝的変異、薬物使用、または炎症性腸疾患やセリアック病 などの特定の病状によって生じることがあります。
ヒスタミン不耐症の有病率は世界的に人口の約 1~3% と推定されていますが、データや診断ツールが不足しているため、実際の有病率を判断するのは困難です。ヒスタミン不耐症のない人でも、大量のヒスタミンを摂取するとヒスタミン毒性を経験する場合があります。ヒスタミンを大量に含む食品 (以下のリストを参照) や DAO の活性を阻害する食品 (アルコールなど) も、ヒスタミン不耐症の症状を悪化させる可能性があります。46サバ科の魚 (最も多いのはマグロやサバ) を適切に冷蔵せずに摂取すると、アレルギー反応に似た症候群が発生します。不適切な冷蔵により、細菌が魚を分解してヒスタミンを形成し、ヒスタミン関連の症状を引き起こす可能性があります。47
ヒスタミン不耐症の症状としては、 以下のものがある45,48。
- 皮膚の紅潮または赤み
- 皮膚の発疹、灼熱感、チクチク感、腫れ
- 低血圧
- 頭痛
- 下痢
- 嘔吐
- 発汗
- 動悸
- 鼻づまり
- 呼吸不全または喘息症状
ヒスタミン含有量の高い食品には以下のものがあります46:
- チェダー、スイス、ブルーチーズなどの熟成チーズ
- ザワークラウト、キムチ、漬物などの発酵食品
- ペパロニ、サラミ、ベーコンなどの塩漬け肉
- マグロ、サバ、アンチョビなどの特定の種類の魚
- 豆腐や醤油などの大豆製品
- バナナ、アボカド、ラズベリーなどの特定の果物
- ピーナッツやカボチャの種などのナッツ類や種子類
|
去痰薬/粘液溶解薬 |
アンブロキソール |
| 非ステロイド性抗炎症薬(NSAID) |
アスピリン、イブプロフェン |
| H2受容体遮断薬 | シメチジン |
| プロキネティクス | メトクロプラミド |
| 抗感染薬 | クラブラン酸、イソニアジド、セフロキシム、セフォチアム、ペンタミジン、クロロキン、ドキシサイクリン、ネオマイシン B、アクリフラビン、D-シクロセリン |
|
気管支拡張薬 |
アミノフィリン、テオフィリン |
|
利尿剤 |
アミロライド、フロセミド |
|
抗うつ薬 |
アミトリプチリン、モノアミン酸化酵素阻害剤 |
|
抗不安薬 |
ジアゼパム、バルビツール酸 |
|
抗精神病薬 |
ハロペリドール |
|
細胞増殖抑制剤 |
シクロホスファミド |
|
降圧剤 |
ベラパミル、ジヒドラジン、アルプレノロール |
|
強心薬 |
ドブタミン、ドーパミン |
|
オピオイド |
ペチジン、モルヒネ、コデイン |
|
鎮痛剤 |
メタミゾール |
|
全身麻酔 |
チオペンタール |
|
筋弛緩剤 |
パンクロニウム、アルクロニウム、D-チューブクラリン |
|
抗不整脈薬 |
プロパフェノン、ベラパミル、キニジン |
|
H1受容体遮断薬 |
プロメタジン |
|
造影剤 |
ヨウ素含有造影剤 |
表2. 低ヒスタミン食中に避けるべき食品49
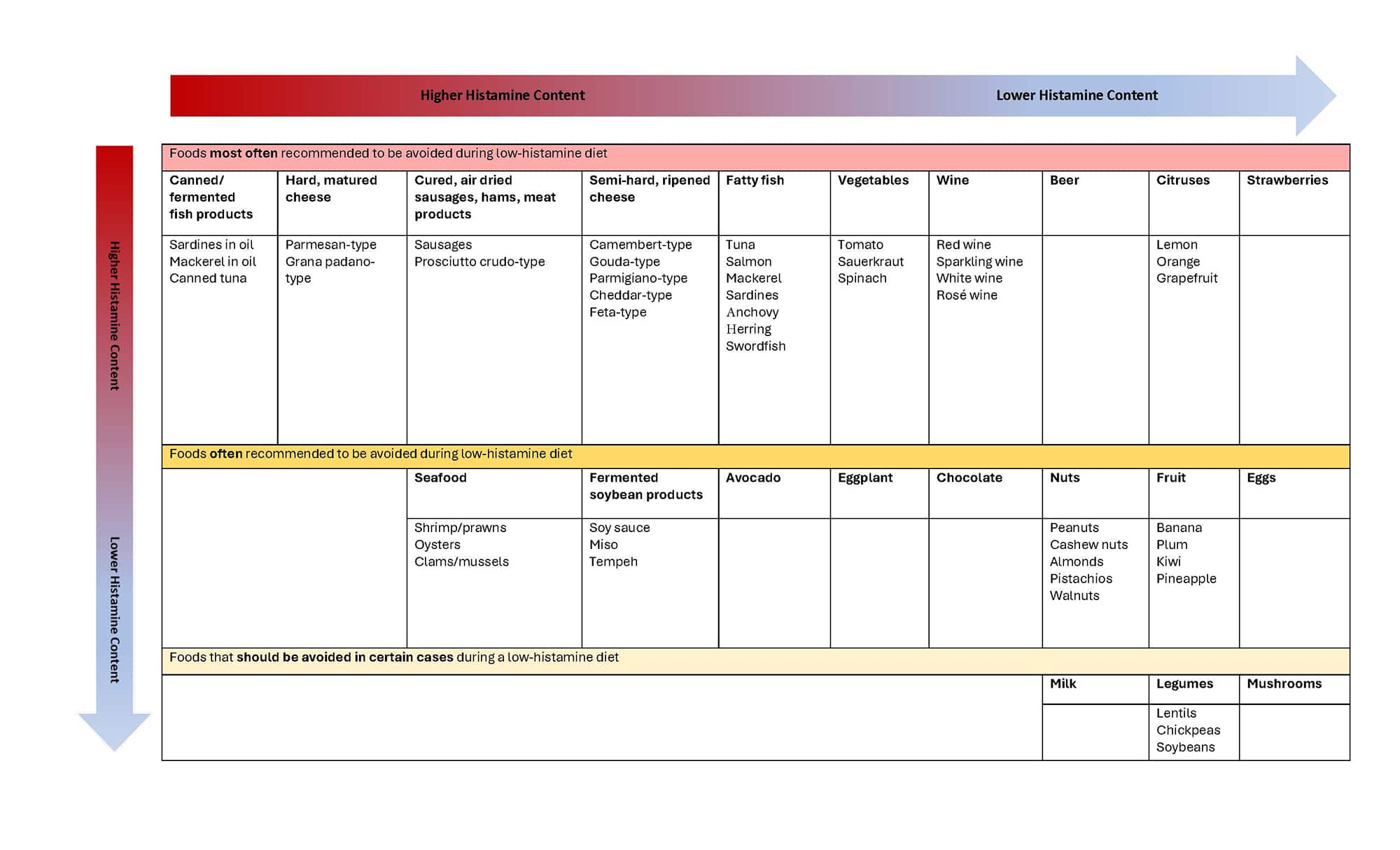
チラミン、プトレッシン、カダベリンなどの他の生体アミンも、ヒスタミン不耐性の症状を引き起こす可能性があります。46プトレッシンとカダベリンは、それぞれアミノ酸のアルギニンとリジンが分解されたときに生成されます。チラミンは、アミノ酸のチロシンが分解されて生成されます。モノアミン酸化酵素 (MAO) の欠乏または阻害は、体内にチラミンが蓄積する原因となります。生体アミンのレベルが上昇すると、DAO が阻害され、体内のヒスタミンの量が増えることもあります。50
関連する遺伝子検査は、23andMe などの消費者直販企業または医師を通じて受けることができます。たとえば、DAO (例: AOC1) または MAO (多くの場合、別の重要な酵素である COMT と連動) の活性に影響を与える遺伝子の変異を検査すると、有益な情報が得られる可能性があります。
その他の要因
食品に対する有害反応の発生には、他にも次のような多くの要因が関係している可能性があります。
自己免疫反応。食物によって引き起こされる免疫反応の中には、本質的に自己免疫性のものがあります。これらの場合、特定の食物または食物成分を摂取したことに反応して免疫系が誤って体自身の組織を攻撃すると、症状が現れることがあります。食物によって引き起こされる可能性のある自己免疫疾患には、セリアック病、クローン病、潰瘍性大腸炎などがあります。51,52
腸管バリア機能の障害。腸管バリア機能障害は「リーキーガット」とも呼ばれ、腸管の内側を覆う細胞間の接合部であるタイトジャンクションが緩んだり損傷したりすることで発症します。タイトジャンクションは腸管の内側にある小さなゲートキーピングの隙間で、栄養素の移動を促進しながら、有害な化合物が血液中に運ばれるのを防ぎます。タイトジャンクションが弱いと、有害な微生物(カンジダ酵母など)、毒素、未消化の食物粒子が腸壁を通り抜けて血流に漏れ出します。53これにより、食物過敏症に関連する症状と同様の全身症状を引き起こす可能性があります。
腸のバリア機能低下の原因となる要因には、反応性の高い食品成分(グルテンなど)への曝露、腸内細菌叢の乱れ、腸内細菌または真菌の過剰増殖、特定の薬剤(NSAIDなど)、セリアック病や炎症性腸疾患などの慢性炎症状態などがあります。54慢性炎症は腸脳軸に沿った神経シグナル伝達を妨害し、マイクロバイオームの不均衡に寄与します。これにより微生物の増殖に理想的な環境が作られ、腸のバリア機能低下や栄養素の吸収低下につながる可能性があります。55
微生物の過剰増殖とグルテン過敏症は、腸漏れの原因となる可能性があります。これらの健康上の問題により、ゾヌリンと呼ばれるタンパク質の放出が誘発されるからです。54ゾヌリンの血中濃度の上昇は、タイトジャンクションの緩みと関連しています。56,57これ により、有害な粒子が血流に漏れ出し、過剰な免疫反応や、鼓腸、腹部のけいれん、膨満感などの腸の問題を引き起こす可能性があります。53
オクルディンは、タイトジャンクションの完全性を維持する役割を果たす膜貫通タンパク質です。一部の研究者は、オクルディンに対する血清中のIgGまたはIgA抗体の測定が腸管バリアの健康状態に関する洞察を提供する可能性があると示唆しています。ただし、このアプローチは厳密な研究で検証される必要があります。58
腸漏れに関連するもう 1 つの潜在的な懸念は、リポ多糖 (LPS) が機能不全の腸バリアから血流に入り、全身性炎症を引き起こす可能性があることです。LPS は脂質と多糖からなる大きな分子で、細菌毒素 (エンドトキシンとも呼ばれる) を構成します。LPS はグラム陰性細菌の外膜の主要成分です。新たな証拠は、LPS がアテローム性動脈硬化症の発症に寄与する炎症反応を引き起こす可能性があることを示唆しています。59-62
いくつかの研究所では、血液中のゾヌリン、オクルディン、LPS のレベルを評価するための新しい革新的な検査を提供しています。
腸内微生物叢。人体の内外に生息する細菌、ウイルス、真菌を含む微生物叢は、消化、免疫、代謝など、人間の健康の多くの側面で重要な役割を果たしています。最近の研究では、腸内微生物叢が食品に対する有害反応の発生や予防にも関与している可能性があることが示唆されています。63腸 内微生物叢が健康であれば、腸の粘液層を維持するのに役立ちますが、繊維質の少ない「西洋式」の食事を続けていると、粘液層にダメージを与える微生物の増殖が促進される可能性があります。64 バランスの取れた食事、プロバイオティクス、その他の介入(消化酵素の補給など)を通じて健康な微生物叢を促進すると、食品不耐症や過敏症を予防または管理するのに役立つ可能性があります。ただし、食品に対する有害反応の発生における微生物叢と免疫システムの多面的な関連性をさらに明らかにするには、さらなる研究が必要です。26
一部の薬剤。特定の薬剤は、食物を消化する身体の能力に影響を及ぼし、腸の機能に影響を及ぼす可能性があります。特に、プロトンポンプ阻害剤(PPI、胃食道逆流症や消化性潰瘍の治療に使用される薬剤の一種)は、食物アレルゲンの消化を妨げ、消化されていない食物アレルゲンの吸収につながる腸のバリア機能の低下に寄与し、微生物叢の不均衡を引き起こすことで、好酸球性食道炎の進行に寄与する可能性があります。65同様 に、制酸薬は胃酸を中和または阻害し、消化されていない食物アレルゲンや、反応を誘発する能力が高まった他の薬剤の成分が循環に入ることを可能にします。66その 結果、人々は薬剤誘発性不耐性を経験したり、腸が食物を処理する速度に問題を抱えたりする可能性があります。これらの問題は、薬剤が消化器系に影響を与え、消化酵素と細菌の自然なバランスを崩す可能性があるために発生します。薬の副作用が現れたり、薬を服用中に食べ物の消化に問題が生じたりした場合は、医師に相談することが重要です。8
精神衛生。神経性無食欲症や神経性過食症などの特定の摂食障害は、身体が食物に反応する方法に影響を与える可能性があります。場合によっては、これらの症状を持つ人は食物に対して心身反応を起こし、吐き気を感じたり、特定の食物が食欲をそそらないと感じたりすることがあります。これらの反応は、食物自体に対する身体的な不耐性ではなく、食物と心理的な関係から生じると考えられています。6,23,67
食事。いくつかの観察証拠は、超加工食品の摂取量の増加が、クローン病や潰瘍性大腸炎などの特定の胃腸疾患のリスク増加と関連していることを示唆しています。68-70超加工食品に含まれるさまざまな添加物(例:過剰な塩分、人工甘味料、赤色40号などの着色料)が、腸内細菌叢を変化させ、腸の炎症を促進する可能性があることが示唆されています。70
環境要因。環境条件は、食品の有害反応に重要な役割を果たす可能性があります。タバコの煙、排気ガス、マイクロプラスチックなどの環境汚染への曝露はすべて、消化管の上皮バリア(保護層)を破壊し、食品アレルギーの発症に寄与する可能性があります。71さらに、パーフルオロアルキルおよびポリフルオロアルキル物質(PFAS)への曝露も問題です。これらの物質は、免疫毒性効果を発揮すると思われる有機化合物のクラスに属し、分解されにくい堅牢な炭素-フッ素構造のため、環境中に残留します。一部の人にとって、PFAS への曝露は、自己申告による食品アレルギーの発生率の増加につながります。72
遺伝と家族歴。遺伝は、食物を消化するのに必要な酵素を体内で十分に生成できるかどうか、あるいは食物を異物と誤認する可能性が高いかどうかに影響します。これらの要因は、食物不耐症や食物アレルギーの発症に寄与します。73
年齢。時間が経つにつれて、体内の酵素の生産量が減少し、特定の食品を効率的に消化することが困難になることがあります。これは、成人の乳糖不耐症などの副作用につながる可能性があります。8 カフェインなど、他の過敏症のリスクも年齢とともに増加する可能性があります。74
膵外分泌機能不全。膵外分泌機能不全 (EPI) は食物反応ではありませんが、食物反応の症状に似た症状を示すことがあるため、そのような症状を経験していると思われる人は考慮する必要があります。EPI の症状には、腹痛、ガスや膨満感、下痢、胃痛、脂肪便 (脂肪分が多く悪臭のある便) などがあり、食物反応の症状と重複したり、同時に発生することがあります。EPI は、食物を適切に分解するのに十分な消化酵素 (リパーゼ、アミラーゼ、プロテアーゼ) を膵臓が生成しない場合に発生します。酵素生成が減少する主な原因は、セリアック病、糖尿病、炎症性腸疾患、膵臓がんなどのさまざまな状態によって生じる膵臓の炎症です。75
サリチル酸塩。サリチル酸塩は、植物が昆虫や病気に対する防御戦略の一環として生成する化学物質で、さまざまな食品に含まれています。ほとんどの人はサリチル酸塩を摂取しても副作用がなく、抗炎症作用やその他の健康上の利点さえ得られます。しかし、サリチル酸塩に過敏な人もいます。このような人の場合、サリチル酸塩は食品の反応に似た症状を引き起こす可能性があります。サリチル酸塩不耐症の一般的な症状には、鼻づまり、副鼻腔感染症、鼻茸、下痢、胃腸炎/大腸炎、じんましんなどがあります。サリチル酸塩を含まない食事やサリチル酸塩の摂取量を減らした食事を試すことで、過敏症かどうかの判断に役立つ場合があります。76
亜硫酸塩。亜硫酸塩は食品、飲料、医薬品の保存に使用される化学物質で、ブドウや熟成チーズに自然に含まれています。亜硫酸塩は、ドライフルーツやワインなどの食品にも腐敗防止のために添加されています。亜硫酸塩に対する過敏症は、食品の反応と混同されることもあります。典型的な症状には、じんましん、皮膚の腫れ、鼻づまり、低血圧、顔面紅潮、下痢、喘鳴、咳などがあります。亜硫酸塩は、喘息患者に気道狭窄を引き起こすこともあります。亜硫酸塩を多く含む食品には、ドライフルーツ、ワイン、アップルサイダー、缶詰野菜、漬物、ポテトチップス、ビール、お茶、一部の焼き菓子などがあります。77
レクチン。レクチンは、一部の人に食物反応を引き起こすという主張により、最近注目を集めています。植物が害虫や病原菌から身を守るために生成するこれらのタンパク質は、さまざまな食品、特にトマト、ピーマン、ジャガイモ、ナスなどのナス科の植物に含まれています。この理論では、一部の人はレクチンを分解するのが難しいため、消化不良、栄養吸収、胃腸炎、腸内微生物叢の破壊につながり、腸漏れや全身性炎症に寄与し、自己免疫の問題を引き起こす可能性があると提唱されています。
しかし、レクチン過敏症は科学的研究が限られており、議論の余地のあるトピックです。78ほとんどの人は、レクチンを含む食品を問題なく摂取できます。それでも、レクチンを含まない食事を取り入れた後、胃腸と全身の健康が大幅に改善したと報告する人もいます。症状の原因がレクチンであるかどうかを判断するには、10~14 日間レクチンを含まない食事を試し、変化を観察します。改善が見られない場合は、他の原因の可能性を考慮する必要があります。
3食品反応の評価と診断

食物不耐症、アレルギー、過敏症は診断が難しい場合があり、軽い不快感から重度のアレルギー反応まで、さまざまな症状を引き起こす可能性があります。医師は身体検査を実施し、個人の病歴を考慮するだけでなく、診断テストの結果を使用して、有害な食物反応の根本的な原因を特定することもできます。現在利用可能なテストを理解することは、個人と医療提供者が診断と治療について情報に基づいた決定を下すのに役立ち、最終的にはこれらの症状に苦しむ人々の生活の質の向上につながります。73
食品が反応を引き起こす可能性のあるすべての方法を特定できる、完璧なアレルギー、不耐性、または感受性検査は存在しないことを理解することが重要です。利用可能なさまざまな検査はすべて異なる情報を提供し、個人が食品に悪影響を及ぼす可能性のあるさまざまな方法を調べます。たとえば、ある人は牛乳に対する IgE 反応が陽性であっても、牛乳に対する IgG/IgA 反応の上昇を示さず、不耐性 (例: 乳糖不耐性) もありません。牛乳に反応することがわかっている別の人は、IgE アレルギー反応が陰性であっても、IgG/IgA 感受性が陽性であり、乳糖不耐性である可能性があります。さらに別の人は、IgE、IgG、および IgA 反応が陰性であっても、乳糖不耐性であり、重大な胃腸症状を示す可能性があります。結局のところ、1 つの検査ですべての答えが得られるわけではありません。各検査には長所と短所があり、各検査は食品反応の潜在的な理由に関して異なる情報を提供します。
共通テスト
皮膚プリックテストとアトピーパッチテスト。皮膚プリックテストとアトピーパッチテストは、アレルギー専門医の指導の下で実施される、食物アレルギー(および環境アレルギー)の一般的な診断テストです。73皮膚プリックテストでは、アレルゲンを含んだ針で皮膚を刺して、少量の食物アレルゲンを皮膚に置きます。その食物にアレルギーがある場合は、その部位に隆起した腫れやじんましんが現れます。このテストは、IgE 媒介食物アレルギーの患者における原因食物の特定に役立ち、プリックテストに対する反応の重症度は通常、食物アレルギーの重症度と一致します。6,38
ただし、皮膚プリックテストにはいくつかの制限があることに注意することが重要です。たとえば、このテストでは、IgE を介さない食物アレルギーを検出できない場合があります。さらに、皮膚プリックテストの結果が陽性であっても、特定の食品を摂取すると必ずしも有害反応が起こるとは予測できません。その逆も同様です。さらに、皮膚プリックテストに使用される方法と検査用品は、検査キット間で標準化されていないため、再検査時に結果が一貫していない可能性があります。皮膚プリックテストは、重度の湿疹のある人や最近抗ヒスタミン薬を服用した人には適さない場合があります。これらの要因は、検査の精度に影響を与える可能性があるためです。湿疹など、皮膚に影響を与える炎症性疾患が広範囲に及ぶ人には、皮膚以外の経路でアレルギー検査を行うことが推奨される場合があります。79-82
アトピーパッチテストでは、通常、アレルゲンを含むパッチまたは包帯を貼付して、潜在的な食物アレルゲンを皮膚に 48 ~ 72 時間保持します。次に、パッチを貼付した皮膚の反応を調べることで、テスト結果を「読み取り」ます。このテストは、非 IgE 媒介性アレルギーや混合型アレルギーなど、発症に時間がかかる食物反応の特定に役立ちます。6パッチテスト法は、皮膚プリックテストが陰性であったが、医師がアレルギーの疑いを残している場合にも使用されることがあります。83
皮膚プリックテストとアトピーパッチテストはどちらも食物アレルギーの潜在的な原因を特定するのに有用ですが、摂取した食物に対して人が反応するかどうかを必ずしも予測できるわけではなく、除去食を設計する際には単独で使用すべきではありません。20
経口食物負荷試験。食物負荷試験は、食物不耐性、過敏症、アレルギーを特定するための重要な診断ツールですが、時間的制約のため、あまり使用されていません。この試験では、医師の監督下で疑わしい食物を徐々に摂取量を増やし、有害反応がないか監視します。84食物 負荷試験は、皮膚テストや血液テストで結論が出ない場合、たとえば、他のテストでは診断が難しい非 IgE 媒介食物アレルギーの診断を確認する場合に使用できます。また、食物アレルギーが成長して治ったかどうかを判断したり、反応が起こる閾値を特定したりするためにも使用されます。85
除去と再導入。除去食は、有害反応を引き起こす原因となる食品、特に IgE 媒介ではないと考えられる食品反応を特定する最良の方法の 1 つです。しかし、ほとんどの人々の忙しい生活スタイルと、必要な準備の多さを考えると、除去食を完了するのは困難です。食品反応のテストとして使用する場合、有害反応を引き起こす疑いのある食品は、2 ~ 4 週間、個人の食事から除去されます。食品除去には、一般的に 3 つのレベルがあります86 :
- レベル 1: 単純な除去食 (例: グルテンフリー、乳製品フリー)
- レベル2: 中程度の強度の除去食(例:低FODMAP)
- レベル3: 少食ダイエット(限られた期間の厳格なダイエット)
除去食のレベルは、除去する疑わしい食品の数によって異なります。除去段階の後、個々の食品が一度に 1 つずつ食事に戻されます。反応が発生した場合、有害反応を引き起こした食品は除去され、食事は除去段階に戻され、体が反応から回復する時間を与えます。最後の反応の症状が治まったら、次の潜在的なトリガー食品が再導入されます。除去食は、すべての疑わしい食品が検査されるまで、これらの除去、再導入、回復段階を経て継続されます。6
これらの食事療法は理論上は簡単ですが、特定の食品を除去すると栄養不足になる可能性があり、長期的な解決策というよりは短期的な手段であるため、このプロセスでは食物反応の管理に経験のある臨床医に相談することをお勧めします。また、経験豊富な臨床医の指導なしに除去食を実施した場合、食物反応の自己診断が不正確になる可能性があります。6
胃腸の症状に対処するために主に設計された除去食の 1 つに、低 FODMAP 食があります。この食事では、乳製品、穀物、特定の果物や野菜などの高 FODMAP 食品を除去し、どの特定の FODMAP 食品が有害反応を引き起こすかを調べることを目的としています。これにより、医師や登録栄養士は、栄養を犠牲にすることなく、食品過敏症や食物反応のある人向けにカスタマイズされた食事を設計できます。6,87
血清免疫グロブリン E (IgE) 検査。総免疫グロブリン E (IgE) 血液検査では、血液中の IgE 抗体の総量を調べます。この検査は、個人の免疫系がアレルギー反応を起こしやすい状態にあるかどうかを判断するのに役立ちます。ただし、総 IgE 検査では、血液中の IgE レベルが高いことやアレルギー反応の原因となっている特定の食品を特定することはできません。6
放射性アレルゲン吸着試験 (RAST) は、アレルゲン特異的 IgE 検査で、タラ、卵白、大豆に含まれるタンパク質などのアレルゲン特異的 IgE を認識する血液中の IgE 抗体を探します。この検査は、食品が反応を引き起こす可能性があるかどうかを判断するのに役立ちますが、食品に対する将来の反応を診断または予測するのにはそれほど役立ちません。ただし、RAST は有用で標準化されており、除去および再導入試験や食物負荷試験の検査対象食品の選択など、他の検査のガイドとして役立ちます。38,88
アレルギー専門医の中には RAST を診療に使用している人もいますが、より多くの医師が、蛍光酵素免疫測定法 [FEIA] 技術を利用した ImmunoCap 特異的 IgE 検査やその他の酵素結合免疫吸着測定法 (ELISA) などの新しい IgE 検査に切り替えています。ImmunoCAP 検査は、アレルギー特異的検査の「次世代」です。ImmunoCAP のような新しい検査方法は、古い方法よりも IgE 媒介アレルギー反応の効力をよりよく反映する可能性があります。89
アレルゲン特異的 IgE 検査のより具体的なバージョンは、成分分解診断 (CRD) 検査です。この検査では、個々のアレルギー分子に特異的な IgE 抗体を特定できます。6たとえば、牛乳が陽性を示した場合、アレルギーを引き起こす可能性のある牛乳の個々の成分 (ラクトアルブミン、ラクトグロブリン、カゼインなど) の検査が続行されます。ただし、CRD 検査は、食物アレルギーの日常的な診断と管理で臨床的にはあまり使用されていません。90
IgE レベルを測定する方法は多数ありますが、IgE 検査で必ずしもアレルゲン特異的 IgE が検出されるとは限りません。IgE 検査は役立ちますが、食物反応の原因を特定するには他の検査を行う必要がある場合があります。
水素呼気検査。水素呼気検査は、特に乳糖や果糖に関連する食物不耐性を特定するために時々使用される診断ツールです。これらの検査では、乳糖または果糖を含む溶液を飲み、呼気中の水素レベルを測定します。体が乳糖または果糖を消化できない場合、消化されなかった糖は不適切に発酵し、過剰な水素ガスが生成され、それが呼気を通じて排出されます。呼気中の水素レベルが上昇すると、検査した特定の糖に対して不耐性がある可能性があります。25、27、28
水素呼気検査は必ずしも信頼できるわけではなく、偽陽性または偽陰性の結果が出る可能性があることに注意することが重要です。さらに、特定の症状( 過敏性腸症候群 [IBS]や炎症性腸疾患など)のある人には適さない場合があります。これらの症状は検査の精度に影響を与える可能性があるためです。ただし、結果を注意深く読むと、役立つ実用的な情報が得られることがよくあります。多くの場合、医療提供者は、食品不耐性を正確に診断するために、さまざまな診断検査の組み合わせを推奨する場合があります。25
内視鏡検査と生検。一部の疾患では、診断のために、影響を受けた消化管組織の内視鏡検査と生検が必要です。内視鏡検査は、内視鏡(先端にカメラとライトが付いた細長い柔軟なチューブ)を使用して体内を検査する医療処置です。内視鏡検査中、医師はカメラを使用して、炎症、出血、腫瘍などの異常や疾患の兆候を探します。医師は、組織サンプル(生検)を採取したり、ポリープの除去などの処置を行うこともできます。内視鏡検査、場合によっては生検が必要となる疾患には、EoE、食物タンパク質誘発症候群、セリアック病などがあります。27,88極端なケースでは、組織内の酵素レベルを測定する生検によって、一部の食物不耐症を診断できます。27,45食物過敏症のほとんどの症例では、内視鏡検査と生検は不要または診断に適応されません。 EoE などの食物反応の場合には、診断に食道生検が必要ですが、これは食物過敏症の標準的な診断手順ではありません。91
追加のテストオプション
免疫グロブリン G (IgG) 検査。食品抗原のパネルを標的とした免疫グロブリン G (IgG) 抗体を測定する血液検査は、食品過敏症の潜在的な誘因を特定する方法として、一部の革新的な医療従事者によって提案されています。
IgG 抗体は、B 細胞によって生成される免疫システムの重要な構成要素です。微生物病原体からの防御、ワクチン接種による免疫誘導、非病原性抗原に対する耐性確保に関与しています。同時に、一部の自己免疫疾患や炎症性疾患の発症にも関与しています。その機能は複雑で、状況に依存します。92
通常、体は、一般的な食事摂取時に、食物抗原に対する IgG 抗体を生成します。IgG 食物過敏症検査に関する研究の中心にあるのは、これらの食物を標的とする IgG 抗体が引き起こす免疫反応の種類、つまり耐性 (非反応性/非炎症性) または不耐性 (反応性または炎症性) です。このトピックに関する研究は複雑で不完全ですが、IgG 抗体によって調整される反応の種類は、いくつかの要因 (例: 個人間の遺伝的変異、抗原曝露の経路、用量、期間、および基礎にある炎症性疾患) によって異なることは明らかです。
IgG には、IgG1、IgG2、IgG3、IgG4 の 4 つのサブクラスまたはアイソタイプがあります。IgG アイソタイプはそれぞれ、抗原に対する免疫応答や耐性にさまざまな影響を及ぼします。たとえば、IgG4 抗体が IgE を介したアレルギー応答を軽減するという確固たる証拠があります。この効果は、IgG4 が IgE 受容体の結合を阻害することと、Fc-γ 受容体 II-β (FcγRIIβ) を介した IgG4 シグナル伝達によって媒介される抗炎症効果によって部分的に生じます。93-95 IgGアイソタイプ 1 および 3 は、補体免疫応答を活性化する能力が高いことから、炎症誘発性であるとよく説明されています (IgG2 は補体を弱く活性化するだけであり、IgG4 は補体を活性化しません)。しかし、最近の証拠では、IgG1~3(特にIgG1)も、一部の細胞型におけるFcγRIIβシグナル伝達を介して、抗原に対する炎症性アレルギー反応を打ち消すことができることが明らかになっています。IgGアイソタイプ1、3、4は、IgG2よりもFcγRIIβに対する結合親和性が高いことが報告されています。92,94興味深いことに 、食物アレルギーに対する経口免疫療法はIgG1~4レベルの上昇を引き起こし、IgG産生の増加(すべてのアイソタイプ)は、特定の食物抗原に対する反応性免疫から寛容性免疫への移行の特徴であることを示唆しています。93,94食事で一般的に遭遇する食物抗原に対する免疫寛容におけるIgG1~3の役割をより詳細に特徴付けるための研究が進行中です。
IgG 血液検査の支持者は、歴史的に IgG サブクラス 4 つすべてを検査するか、IgG4 のみを検査することを推奨してきました。しかし、食物アレルギーにおける IgG4 の保護的役割が文献で明確に確立されるにつれて、IgG 食物過敏症検査の支持者は IgG アイソタイプ 1~3 のみの評価を提案し始めました。2024 年半ばの時点では、両方のタイプの検査が市場で入手可能です。
IgG 検査の支持者は、過敏性腸症候群や片頭痛などの症状に対する IgG 誘導除去食のメリットに関する複数の公表されたレポートを指摘し88,96-104、一部の代替医療の臨床医は、特に除去食のガイドとして、食物過敏症 (不耐性やアレルギーに関連しない食物反応) に対する IgG 検査の価値を認識しています。これらの臨床医は、血中 IgG レベルの上昇が患者の腸の健康に関する洞察を提供する可能性があることも示唆することがあります。これらの臨床医が IgG 検査が正当であると感じる例としては、患者が特定のアレルギーや不耐性を除外したにもかかわらず、継続的に認識されている有害な食物反応を報告した場合が挙げられます。このような場合、IgG 検査によって患者が頻繁に食べる食品を特定することで、臨床医が治療上の試験的な除去食を作成するのに役立ちます。逆に、IgG 検査の使用を推奨しない臨床医は、食事日記や、患者の特定の懸念に関連して問題となることが多い 1 種類または数種類の食品の除去など、他の手段で導かれる食生活の変更を追求することを好む場合があります。他の臨床医は、地中海ダイエットなど、一般的に健康的な食事パターンを患者が順守できるように支援することを好む場合があります。推奨されるアプローチは、臨床医の経験によって異なります。105-110一部 の研究者と臨床医は、IgG 抗体が、場合によっては IgE を介さない食物過敏症を引き起こしたり、その一因になったりする可能性があると示唆しています。特に、EoE の状況で IgG が関与している可能性があるという証拠が近年いくつか出てきました。いくつかの研究では、血中 IgG 検査が除去食の設計にも役立つことがわかりました。IgG 検査に基づく除去食は、小規模な研究で下痢型過敏性腸症候群 (IBS-D) と片頭痛の症状を改善することが示されています。片頭痛患者を登録し、IgG 検査に基づいて除去食を実施したある研究では、IgG に基づく除去食により、4 週間で片頭痛のような頭痛の回数が減ったものの、12 週間では減らなかったことがわかりました。
好塩基球および肥満細胞活性化試験。好塩基球活性化試験では、アレルギー反応の原因となる免疫細胞の一つである好塩基球の採血を行います。採血後、好塩基球を特定のアレルゲンにさらし、好塩基球反応の程度を測定します。111
肥満細胞活性化テストは好塩基球活性化テストに似ていますが、実験室で個人の血清(血液の透明な部分)を肥満細胞に加える点が異なります。肥満細胞は即時アレルギー反応に関与する免疫細胞の一種で、特定の寄生虫や細菌に対する免疫システムの反応を制御する役割も果たします。血清で処理された肥満細胞がアレルゲンにさらされたときに活性化した場合、このテストは陽性となります。111
好塩基球活性化テストと肥満細胞活性化テストはどちらも、個人が特定の食品に反応するかどうかを予測するのに役立つ可能性があります。ただし、これらのテストを標準化し、より広く利用できるようにするためには、さらなる研究が必要です。90,111
遺伝子検査。遺伝子検査は、食物不耐症やアレルギーを診断する比較的新しい方法です。この検査では、個人の DNA を分析して、食物不耐症やアレルギーを発症するリスクの増加に関連する遺伝子変異を特定します。たとえば、遺伝子検査は、個人がセリアック病を発症するリスクがあるかどうかを判断するのに役立ちます。51,112遺伝子検査では、ヒスタミン、フルクトース、またはラクトース不耐症の個人を特定することもできますが、これは臨床診療ではあまり行われていません。23,45 ただし、近年では、消費者に直接提供される遺伝子検査がさらに増えています 。
遺伝子検査は、食物不耐性やアレルギーに対する個人の遺伝的リスクに関する有用な情報を提供しますが、不耐性やアレルギーを発症するかどうかを明確に予測するものではありません。つまり、特定の不耐性やアレルギーに関連する遺伝子変異を持っているからといって、必ずしもその個人がその症状を発症するわけではありませんが、その症状を発症する確率が高いことは明らかです。112さらに、食品に対する有害反応の発症に寄与する可能性のある遺伝子の多くはまだ不明です。113これらの理由から、遺伝子検査は他の診断アプローチと併用して、個人のリスクをより包括的に理解するために使用できます。111,114
腸バリア検査。人の腸がどの程度透過性があるか、つまり「漏れやすい」かを測定するための標準化された検査はありません。さまざまな化合物や分子が腸から血流に「漏れる」可能性があるかどうかを判断するために設計された検査が開発中です。これには、血液中の細菌成分を調べる血液検査や、腸から漏れたさまざまな種類の糖を調べる尿検査が含まれます。特に、腸バリアパネル検査は、ゾヌリン、オクルディン、カンジダアルビカンス、LPS など、腸バリア機能の調節に寄与するか、腸バリアの透過性を示す特定のマーカーを検出します。これらのパネルの結果は、腸漏れの存在を評価し、腸バリア機能をモニタリングする手段を提供します。生検と内視鏡検査も、腸バリアが損傷しているかどうかを判断するのに役立ちます。115これらの検査の一部はまだ実験段階にあり、その他は市販されています。資格のある医療従事者は、特定のケースで腸バリア検査が適切かどうかを判断するのに役立ちます。
食物アレルギーの原因を診断するための検査は数多くありますが、原因によっては 1 回の検査で明確に診断することが困難または不可能なものもあります。すべての食物アレルギー/過敏症/反応/不耐性を検査できる 1 回の検査は存在しません。なぜなら、さまざまな検査が、食物に対する体のさまざまな反応を評価しているからです。各検査は、免疫系と体の反応に関するさまざまな情報を提供します。ヒスタミン不耐性などの一部の症状については、現在、診断に使用できる検査はありません。他の原因が排除された場合にのみ、ヒスタミン不耐性が診断として考慮されます。23,45資格 のある医療専門家は、正確な診断につながる診断手順の種類と組み合わせの決定にも役立ちます。
4食生活とライフスタイルの変化
食物過敏症、不耐症、アレルギーはさまざまな不快な症状を引き起こす可能性があり、診断や治療が難しい場合があります。しかし、食生活やライフスタイルを少し変えるだけで、症状を緩和し、全体的な健康状態を改善できます。役立つヒントをいくつかご紹介します。
食物アレルギーの第一選択治療は、原因となる食物を食事から排除することです。多くの場合、これで問題全体が解決し、それ以上の治療(医療など)は必要ありません。しかし、一般的な食物や原材料に過敏症のある人にとっては、回避が難しい場合があります。たとえば、ピーナッツは、同じ施設で加工された食品を汚染する可能性があります。これにより、ピーナッツアレルギーのある人の食事から、ピーナッツを含まない食品さえ排除される可能性があります。5さらに 、特定の食物を排除すると、特に子供の場合、ビタミンや栄養素の欠乏につながる可能性があります。たとえば、乳糖不耐症の人は、乳製品がこれらの栄養素の主な供給源であるため、食事にカルシウムとカリウム、ビタミン B12 と D を補給する必要があるかもしれません。6,28,116
食事から食品を排除または制限することを決定する際には、通常起こる反応の重症度を考慮する必要があります。免疫介在性でない不耐症の人は、少量の誘発食品を摂取しても問題ない場合があります。反応の重症度は、誘発食品を摂取した量によって決まることが多いためです。たとえば、乳糖不耐症の人の多くは、他の食品と一緒に摂取した場合、症状を経験することなく、一度に最大 12 グラムの乳糖 (約 200~250 mL、または約 8 液量オンスの牛乳に相当) を摂取できます。25いくつかの研究では、ヨーグルトなどの発酵乳製品は、細菌含有量のために他の種類の乳製品よりも消化しやすい可能性があることが示唆されています。細菌には乳糖の消化を助けるラクターゼ酵素が含まれている可能性がありますが、個人によって反応が異なる場合があり、追加の研究が必要です。25,117-119
食物アレルギーやセリアック病などの免疫介在性過敏症の場合、原因となる食品を食事から完全に排除する必要があることがよくあります。セリアック病患者がグルテンを摂取すると、腸に修復不可能な損傷を与える可能性があるため、グルテンを含む食品はすべて避ける必要があります。食物アレルギーはアナフィラキシーを引き起こし、死に至る可能性もあります。さらに、既知の原因食品に関連する一部の食品は、交差反応性 IgE 抗体による反応を引き起こす可能性があるため、避けるべきです。38
副作用に関連する一般的な食品を避けたり、代替したりするのは難しいことが多いため、一般的な誘因といくつかの代替食品の表を用意しました。
| 表3. 一般的な食物反応の誘因と代替手段 | ||
|---|---|---|
| トリガー | 一般的な情報源 | 潜在的な代替案 |
| カフェイン |
コーヒー、紅茶、チョコレート、エナジードリンク、一部の薬 |
ハーブティー、カフェイン抜きコーヒー、カフェインフリーのソフトドリンク |
| 乳糖と乳製品 |
牛乳、チーズ、ヨーグルト、アイスクリーム、バター、クリーム、そして多くの焼き菓子、ソース、加工食品 |
乳糖を含まない牛乳または牛乳代替品(豆乳、アーモンドミルク、ココナッツミルク、オートミルクなど) |
| 卵 |
卵、焼き菓子、パスタ、マヨネーズ、カスタード、メレンゲ、その他多くの加工食品 |
アップルソース、マッシュバナナ、絹ごし豆腐、市販の卵代替品などの卵代替品 豆類、ナッツ類、種子類などの代替タンパク質源 |
| フルクトース |
リンゴ、ナシ、マンゴー、スイカなどの多くの果物 多くの加工食品や甘味飲料に含まれる蜂蜜、アガベシロップ、高果糖コーンシロップ |
イチゴ、オレンジ、バナナ、アボカド、キウイ、パイナップルなどの低果糖果物 |
| ピーナッツ |
ピーナッツ、ピーナッツバター、焼き菓子、多くの加工食品 |
豆、レンズ豆、エンドウ豆、大豆製品などの代替タンパク質源 アーモンド、カシューナッツ、ヒマワリの種から作られたナッツバター |
| 大豆 |
豆乳、豆腐、テンペ、醤油、味噌、枝豆、その他多くの加工食品 |
豆、レンズ豆、エンドウ豆、ナッツなどの代替タンパク質源 醤油の代わりにココナッツアミノ |
| 生の果物や野菜 |
パイナップル、マンゴー、カシューナッツ、リンゴ、ナシ、モモ、プラム、サクランボ、キウイ、バナナ、メロン、トマト、セロリ、ニンジン、ジャガイモ |
調理済みまたは缶詰の果物と野菜 誘発食品と同じ植物科ではない代替の新鮮な果物や野菜 |
| 小麦 |
パン、パスタ、シリアル、クラッカー、焼き菓子、ビール、醤油、サラダドレッシング、ソース、グレービーソース グルテンを含む小麦以外の穀物:大麦、ライ麦、ライ小麦、ブルグル、クスクス |
グルテン不耐症: 米、キヌア、そば、オート麦などのグルテンフリー穀物(グルテンフリー認定品) 小麦アレルギー:米、トウモロコシ、キヌアなどの小麦を含まない穀物 醤油の代わりにココナッツアミノ |
健康的でバランスのとれた食生活を取り入れることも、食べ物に対する否定的な反応を減らすのに役立ちます。さまざまな果物、野菜、全粒穀物、赤身のタンパク質、健康的な脂肪を摂取すると、腸の健康をサポートし、炎症を軽減するのに役立ちます。また、食事にプロバイオティクスとプレバイオティクスを取り入れて、食べ物を適切に分解するのに役立つ有益な腸内細菌の成長を促進することも役立つ場合があります。発酵食品は、食物過敏症に苦しむ人々の胃腸にメリットをもたらす可能性があります。いくつかの研究では、ケフィア(ケフィアグレインと牛、羊、または山羊のミルクから作られる発酵飲料)は、乳糖不耐症の人にも耐えられる可能性があることが示されています。ケフィアの細菌は乳糖を消費するため、体が消化しやすくなります。120発酵食品が食物アレルギー、腸内微生物叢、免疫システムの調節に与える影響に関する研究が進行中です。
最後に、ストレスレベルを下げ、十分な睡眠をとるなどの生活習慣を変えることも、症状や全体的な健康を改善するのに役立つ可能性があります。121,122十分 な睡眠をとることも重要です。研究によると、例えばピーナッツアレルギーを持つ人の場合、睡眠不足はアレルゲン刺激に対する反応の重症度を高める可能性があることが示されています。123
まとめると、食生活やライフスタイルを変えることで、食物過敏症、不耐症、アレルギーのある人の症状を緩和し、全体的な健康状態を改善することができます。原因となる食品を特定して避け、健康的でバランスの取れた食事を取り入れ、ライフスタイルを変えることは、症状の改善と全体的な健康状態の改善につながります。
5栄養素
注意: ここで説明する栄養素は、真の食物アレルギーを解消するものではありません。食物アレルギーと診断された人は、アレルギー専門医または免疫学者と緊密に連携し、サプリメントを摂取すればアレルギーのある食物を摂取できると決して考えないでください。
腸内微生物叢のサポート
プロバイオティクス。現代人の腸内細菌叢の変化は、おそらく食物アレルギーの有病率の増加に寄与している。124観察研究により、食物アレルギーのある人とない人の間では、腸内細菌叢の量的および質的な違いが特定されている。その結果、食物アレルギーや過敏症のある人にとって、腸内細菌叢の健康と多様性をサポートすることは合理的である。125しかし、細菌叢を標的とする戦略は数多くあるため、プロバイオティクスの補給など、特定の介入に関する証拠は一般に予備的なものである。それでも、食物過敏症のある人にとっては、腸内細菌叢をサポートするための措置を講じることが賢明である。そのような措置の 1 つがプロバイオティクスの補給である。しかし、2023 年後半の時点で、食物アレルギーの文脈でのプロバイオティクスに関する研究のほとんどは、主に牛乳やピーナッツアレルギーのある子供を対象としている。この文脈では、予備的ではあるが、研究は有望である。126,127
ラクトバチルス カゼイ、ビフィドバクテリウム ラクティス、L. ラムノサス、および/またはB. ビフィダム を含むさまざまなプロバイオティクス種は、牛乳アレルギーのある小児に免疫寛容を誘発する可能性があることが報告されています。128,129ある試験では、牛乳アレルギーのある 1~18 歳の小児 61 名が登録され、1 つのグループには経口免疫療法とプロバイオティクスの補給が、もう 1 つのグループには経口免疫療法とプラセボが割り付けられました。Lactiplantibacillus plantarum YIT 0132 の補給により、24 週間後に牛乳に対する寛容性がわずかに改善されました。130多施設ランダム化比較試験では、除去食治療を受けていた牛乳アレルギーとアトピー性皮膚炎を患う 151 名の小児が、プラセボまたはL. rhamnosus ŁOCK 0900、L. rhamnosus ŁOCK 0908、およびL. casei ŁOCK 0918 株の細菌 10 億個を毎日補給しました。プロバイオティクスを摂取した参加者は、プラセボを摂取した参加者と比較して、3 か月でアトピー性皮膚炎の症状が著しく改善したことがわかりました。131牛乳アレルギーのある 330 名の小児を評価したコホート研究では、L. rhamnosus GG 補給と高度に加水分解されたカゼインタンパク質を併用すると、カゼイン単独と比較して、機能性胃腸障害の有病率が減少することがわかりました。132他の証拠も、L. rhamnosus GGの補給が牛乳アレルギーのある子供に有益である可能性があることを示唆しています。133,134
注目すべきは、個人の遺伝的/生化学的差異により、どのプロバイオティクスもすべての人に効くわけではないということです。ある人はプロバイオティクスの 1 株で改善を感じるかもしれませんが、別の人は悪化を感じるかもしれません。各個人にとって最適なプロバイオティクス ブレンドを見つけるには、試行錯誤が必要になる場合があります。
消化サポート
酵素。消化管内の酵素は栄養素の吸収と消化機能を促進します。特定の食物不耐症や過敏症の場合、サプリメントの形で入手できる酵素は、原因となる化合物の消化を改善することで症状を最小限に抑えるのに役立つ場合があります。これらには、アミラーゼ、プロテアーゼ、セルラーゼ、キシロースイソメラーゼ、スクラーゼ、マルターゼ、ラクターゼ、グルテナーゼが含まれ、複合炭水化物、植物性タンパク質、砂糖、ラクトース、グルテンなどのさまざまな摂取化合物の消化をサポートするのに役立ちます。135ラクターゼはラクトース不耐症の人に有用であり、グルテン分解酵素はグルテン過敏症やセリアック病の人のために研究されています。136,137 2023年後半の時点で、セリアック病の唯一の広く受け入れられている治療法はグルテンフリーの食事であることに注意することが重要です。しかし、これらの消化酵素は、胃腸疾患(例:IBS)に関連する食物過敏症に関連する症状を最小限に抑えるのに役立つ可能性があります。135
特定の酵素である AN-PEP ( Aspergillus niger由来のプロリルエンドプロテアーゼ) は、試験管内で研究され、グルテンを分解することが示されています。AN-PEP は、他の市販のプロテアーゼサプリメントと比較して、胃の pH 範囲でグルテンを効果的に分解することが示されています。この試験管内研究では、AN-PEP は 9 種類の免疫原性グルテンペプチドを効果的に分解しましたが、市販の消化酵素サプリメント 5 種類は分解しませんでした。138グルテン過敏症を自覚している18 人の被験者において、グルテンを含むお粥と一緒に AN-PEP を摂取したところ、プラセボと比較して胃と十二指腸のグルテンレベルが大幅に低下しました。この研究では、低用量と高用量の 2 種類の AN-PEP が使用され、低用量の 2 倍の酵素活性が得られました。用量は酵素活性に基づいて決定されました。139小規模な臨床研究から得られた他の証拠も、 AN-PEP が胃の中でグルテンを分解する可能性を裏付けています。140しかし、別の小規模な臨床研究では、AN-PEP を摂取し、管理された条件下でグルテンを摂取したセリアック病患者は、プラセボを摂取した患者と比較して、詳細な検査 (組織学) でセリアック病の品質スコアや腸壁の健康状態に有意な違いは見られませんでした。141グルテン過敏症における AN-PEP 補給の有効性を明らかにするには、さらなる研究が必要です。
このプロトコルの他の箇所で説明されているように、ヒスタミンやその他の生体アミンは食物不耐症の症状に関与している可能性があります。一部の研究者は、「ヒスタミン不耐症」という概念を、胃腸の不快感、頭痛、皮膚の紅潮、くしゃみや鼻水、喘息など、食物過敏症と表現される症状の潜在的な一因として提唱しています。ジアミンオキシダーゼ (DAO) は、腸内のヒスタミン (つまり、食物ヒスタミン) を分解する主な酵素であり、ヒスタミン不耐症は DAO 酵素の活性が相対的に低いことが特徴であると考えられています。46
研究では豚の腎臓由来のDAOサプリメントの効果を調査し、ヒスタミン不耐性と考えられる人々に対して、いくつかの潜在的な利点(例えば、胃腸症状、蕁麻疹、片頭痛の改善)を示唆しています。142-144しかし、最近では、白エンドウ豆( Lathyrus sativus )由来のDAOが動物由来のDAOよりも高い比活性を持ち、ヒスタミン関連の組織損傷を防ぐことが示されました。145,146
腸管バリアの健全性をサポート
「腸漏れ」または腸バリアの完全性障害の概念は、食物過敏症の文脈でよく議論されます。腸バリアの完全性障害が食物過敏症と相関している可能性、または食物過敏症が腸バリアの完全性を損なう可能性があるという証拠がいくつかあります。また、腸バリアの損傷が食物不耐性の増加につながる可能性もあります。しかし、腸漏れが食物過敏症全般の重要な根底にある現象であるかどうかについては、医学文献でコンセンサスが得られていません。また、「腸漏れ」と「食物過敏症」の一貫した定義もないため、潜在的な関連性の理解がさらに複雑になっています。それでも、一部の統合医療従事者や食物過敏症患者は、腸バリアの完全性を改善する措置を講じることで食物過敏症の症状を緩和できたと報告しています。115
このセクションでは、Life Extension の私たちが、腸のバリアの健全性をサポートする可能性のある特定の介入に関する証拠をいくつかまとめました。このセクションで説明されている介入の一部は、主に理論的または間接的な潜在的利益の証拠によってサポートされており、食物過敏症を持つすべての人に役立つとは限りません。また、炎症性腸疾患などの真の炎症性疾患は、「リーキーガット」という用語が通常示唆するものよりも顕著なバリア機能障害を引き起こす可能性があることにも注意してください。基礎にある炎症性疾患のために腸のバリア機能が損なわれている可能性のある人は、消化器専門医に相談する必要があります。115
プロバイオティクス。多くの研究は、さまざまなプロバイオティクス株が腸のバリアの健康をサポートする可能性があることを示唆しています。たとえば、2023年に発表された26件のランダム化比較試験のデータを含むメタ分析の累積的な証拠は、腸の透過性またはバリア機能のいくつかの指標(すなわち、経上皮抵抗、血清ゾヌリン、エンドトキシン、およびLPS)を通じて評価したところ、プロバイオティクスが腸のバリア機能を大幅に改善したことを示しました。メタ分析に含まれる研究ではさまざまなプロバイオティクス株が使用されていましたが、ほとんどの研究ではラクトバチルス属とビフィズス菌 属のプロバイオティクスが含まれ、いくつかの研究ではエンテロコッカス属 とストレプトコッカス属の微生物が含まれていました。147
プレバイオティクス。炭水化物ベースの「プロバイオティクス用食品」であるプレバイオティクスが、腸のバリアの完全性をサポートするのに役立つという証拠もあります。興味深いことに、プレバイオティクスが腸のバリアの完全性に与える潜在的な利点は、微生物依存性と微生物非依存性の両方の効果に関連している可能性があります。腸のバリアの完全性をサポートする可能性のあるプレバイオティクスには、イヌリン、フルクトオリゴ糖、ガラクトオリゴ糖、キシロオリゴ糖などがあります。148
プレバイオティクスの重要性は、消化管マイクロバイオームの性質に関する認識不足のため、過小評価されることが多い。腸内マイクロバイオームの大部分は、酸素の存在下で死滅する嫌気性細菌と、低酸素レベルを必要とする微好気性細菌から構成される。このため、嫌気性または微好気性のプロバイオティクスの製造はほぼ不可能である。これらの必須微生物をサポートするには、糞便移植を受けるか、果物、野菜、複合炭水化物が豊富な地中海食を摂取する必要がある。もう 1 つの選択肢は、有益なビフィズス菌の成長を促進するために、キシロオリゴ糖などの標的プレバイオティクスを摂取することである。消化管マイクロバイオームの約 11% のみが好気性 (酸素を好む) であり、44% が微好気性、45% が嫌気性である。したがって、消化管の健康をサポートする最良の方法は、地中海食とプロバイオティクスおよびプレバイオティクスの両方を組み合わせることである。149
グルタミン。グルタミンは体内で多様な役割を果たすアミノ酸です。グルタミンは「条件付き必須」であると考えられており、つまり、特定の状況、主に異化状態(重篤な病気や全身の生理的ストレスなど)を特徴とする状況ではグルタミンの摂取が必要です。多くの前臨床研究で、グルタミンが腸管バリアの完全性をサポートするメカニズムが特定されています。150,151しかし 、炎症性腸疾患の患者を対象としたヒトの臨床研究の証拠では、グルタミン補給は一般的に効果がないことがわかりました。152一方、1 つの小規模な試験では、グルタミン補給(1 日 3 回 5 グラム)が IBS-D の患者に有益であることがわかりました。153前臨床研究では、IBS-D の患者の結腸生検標本を 10 mmol/L のグルタミンで培養すると、タイトジャンクションタンパク質であるクローディン 1 の発現が増加しました。154しかしながら、経口摂取したグルタミンのほとんどは小腸で吸収されるため、この研究で使用されたグルタミンの濃度が生理学的に関連があるかどうかは不明です。151 全体として、グルタミンが腸管バリアの健康をサポートする可能性があることを示唆するメカニズムの証拠がいくつかあります。
酪酸。短鎖脂肪酸である酪酸は、腸内細菌の代謝産物であり、腸の免疫機能や上皮バリア機能の調節など、いくつかのメカニズムを通じて腸の健康に貢献しています。2019年に発表されたメタアナリシスでは、12の研究のデータを分析し、炎症性腸疾患の患者では酪酸を含むいくつかの短鎖脂肪酸の濃度が低いことがわかりました。特に酪酸に関しては、潰瘍性大腸炎の寛解期の患者は活動期の患者と比較して濃度が高く、クローン病の患者では一般的に低かったです。155 炎症性腸疾患の 患者を対象とした介入研究では、経口投与された酪酸は一般的に炎症を軽減する効果があるのに対し、浣腸で投与された酪酸は効果がまちまちであることが示されています。156マイクロカプセル化された酪酸を12 週間経口補給すると、IBSの患者の症状の一部が軽減されることが示されました。157食物反応に関しては、前臨床的および観察的証拠から酪酸がこの状況で有益である可能性が示唆されているが、さらなる研究が必要である。158-160
クルクミン。スパイスのターメリックの有効成分であるクルクミンは、さまざまな健康状態との関連で研究されてきました。かなりの前臨床的証拠から、クルクミンには腸に影響を与える炎症性疾患を改善する可能性があると示唆されています。炎症の調整と腸のバリア機能の保護は、クルクミンが腸の健康を促進する可能性のあるメカニズムです。161,162一部 の研究者は、クルクミンが腸のバリアの完全性を維持することにより、腸から循環への細菌毒素LPSの放出を減らす能力を、クルクミンの全身的利点の重要なメカニズムとして強調しています。162また、前臨床研究では、クルクミンにはいくつかの免疫調整効果があることが示されており、アレルギーに対する潜在的に有用な介入としてこの化合物への関心が高まっています。163 一部の動物研究では、クルクミンが食物アレルギーに有益である可能性があることが実証されています。164,165あるプラセボ対照臨床試験では、軽度から中等度の潰瘍性大腸炎の患者 50 名が、メサラミン (5-アミノサリチル酸または 5-ASA、潰瘍性大腸炎の治療薬) と 1 日 3 グラムのクルクミンまたはプラセボを 1 か月間投与されました。クルクミンを投与された患者のうち 14 名が 4 週間後に臨床的寛解を達成しましたが、プラセボを投与された患者は 1 名もいませんでした。166
亜鉛-L-カルノシン。キレート化合物の亜鉛-L-カルノシンは、損傷した粘膜に局所的に亜鉛を送達する能力があるため、胃腸疾患の分野で関心を集めています。亜鉛-L-カルノシンは、前臨床研究で胃および腸粘膜損傷の修復を促進することが示されています。いくつかの小規模試験では、さまざまな臨床状況で亜鉛-L-カルノシンが胃または腸粘膜の治癒に有効であることが示されています。167たとえば、胃潰瘍患者 224 名を対象とした多施設臨床試験では、亜鉛-L-カルノシンによる 8 週間の治療が、症状の緩和において粘膜保護薬レバミピドとほぼ同等の効果があることがわかりました。168小規模(n=10)クロスオーバー臨床試験では、胃腸障害を引き起こすことが知られている NSAID インドメタシン(Tivorbex)を 5 日間投与した後、1 日 2 回 37.5 mg の亜鉛-L-カルノシンを投与したところ、腸管透過性が低下しました。169別の小規模試験では、低用量アスピリン誘発性の小腸障害のある 20 人の被験者が、4 週間、亜鉛-L-カルノシン(1 日 150 mg)またはプラセボのいずれかを投与されるよう無作為に割り付けられました。治療後、腸の病変または潰瘍の数は亜鉛-L-カルノシン グループで有意に減少しましたが、プラセボ グループでは減少しませんでした。170健康なボランティアによるさらに別の 14 日間の小規模試験では、亜鉛-L-カルノシン(1 日 2 回 37.5 mg)を単独またはウシ初乳と併用することで、運動誘発性の腸管透過性の上昇が軽減されました。171 3件の試験から得られた証拠は、ヘリコバクター・ピロリ(H.ピロリ)感染症の一般的な治療である3剤併用療法(抗生物質2剤とPPI)に亜鉛-L-カルノシンを追加すると、ピロリ菌の除菌率が向上する可能性があることも示唆している。172 2024年半ばまでに発表された研究では、食物反応に関して亜鉛-L-カルノシンの理論的利点が示唆されているが、さらなる研究が必要である。
オメガ3脂肪酸
オメガ 3 多価不飽和脂肪酸 (PUFA) は、免疫系の反応と炎症経路に影響を与えることが示されています。前臨床研究では、オメガ 3 サプリメントはアレルギー反応を抑制し、症状を改善できることが示唆されています。173さらに、PUFA 由来のプロレゾルビン、リポキシン、マレシン、プロテクチンなどの炎症状態に対する有益な保護効果を持つ可能性のある抗炎症剤です。174
健康的なオメガ 6:オメガ 3 比率 (典型的な西洋の食事で一般的な 20:1 ではなく、4:1 に近い) を維持することは、炎症、アレルギー、自己免疫反応を軽減するための効果的な戦略である可能性があると言われています。175小規模な臨床研究では、ピーナッツアレルギーのある人は、健康な対照群と比較して、アラキドン酸 (オメガ 6) のレベルが高く、オメガ 3 PUFA であるエイコサペンタエン酸 (EPA) とドコサヘキサエン酸 (DHA) のレベルが低いことが示されました。スクリーニングでは、特定の IgE レベルと総 PUFA 濃度の間に逆相関関係があることも示されました。176これらの結果は、PUFA 摂取が慢性アレルギー疾患や食物反応の発生、進行、および治療に果たす役割の証拠を提供します。将来の研究で、食物反応や関連疾患におけるオメガ 3 PUFA の役割が解明されることが期待されます。
ポリフェノール
果物や野菜、またお茶やワインなどの植物由来の食品や飲料に含まれる抗酸化物質であるポリフェノールは、抗炎症作用があることで知られており、さまざまな健康上の懸念との関連で研究されてきました。その抗酸化作用は炎症を軽減するのに役立ち、一部の食品反応の治療に役立つ可能性があります。177-179ポリフェノールは、炎症性腸疾患の症状の改善にも役立つ可能性があります。180,181さらに、ポリフェノールは最近、マイクロバイオームに良い影響を与える重要なプレバイオティクスとして説明されています。摂取すると、プレバイオティクスポリフェノールは有益な細菌の増殖と重要な代謝産物の生成を促進します。182
ポリフェノール は、腸内のタンパク質に結合して免疫細胞がそれらを検知するのを防ぐことで、アレルゲンや食物誘発物質を「隠す」ことができると示唆されている。183,184たとえば、緑茶に含まれるポリフェノールのエピガロカテキンガレート (EGCG) は、試験管内でグルテンに結合し、腸の免疫細胞によるグルテンの認識をブロックすることがわかっている。183,185他 にも多数のポリフェノールが、免疫原性食品タンパク質と相互作用することがわかっているが、ポリフェノールが食品反応に及ぼす臨床的影響については、さらに研究する必要がある。183
食物アレルギーに関しては、特定のポリフェノールに抗炎症作用があり、アレルギー反応を軽減する可能性があることを示唆する予備研究があります。186
緑茶ポリフェノール。2013年のパイロット研究では、毎日 400~800 mg の EGCG を摂取すると、副作用はほとんどなく潰瘍性大腸炎の症状が改善することが分かりました。これは 20 名を対象とした小規模な研究であったため、緑茶ポリフェノールが他の食物反応や関連疾患の治療に使用できるかどうかについてさらなる証拠を得るには、今後、より大規模な参加者を対象とした研究が必要です。187
レスベラトロール。レスベラトロールはブドウ、ベリー、赤ワインに含まれるポリフェノールです。2015 年に実施された小規模な研究では、潰瘍性大腸炎患者に 6 週間毎日 500 mg のレスベラトロールを投与したところ、病気の重症度と患者の生活の質が改善されたことがわかりました。ただし、研究の規模は小さく、参加者は 50 人でした。188
ケルセチン。ケルセチンは、ピーマン、赤玉ねぎ、クランベリー、レタス、コリアンダーなど、さまざまな食品に含まれる最も一般的なフラボノイドの 1 つです。ケルセチンは、肥満細胞と好塩基球の細胞膜を安定化させ、過剰な炎症誘発性メディエーターの放出を防ぐことが in vitro で示されています。189動物実験では 、ケルセチンがアレルギー性鼻炎、アトピー性皮膚炎、その他のアレルギー関連症状の改善に役立つ可能性があることが示唆されています190。ただし、ケルセチンが食物反応やその他の関連症状に有益であるかどうかを判断するには、さらに研究が必要です。
亜鉛
亜鉛は、腸内壁や体全体の免疫機能において中心的な役割を果たす重要なミネラルです。亜鉛のシグナル伝達が適切であれば、肥満細胞、T 細胞、B 細胞、好酸球、好塩基球の活動が制御され、炎症性およびアレルギー性の免疫活動が制限されます。191,192亜鉛欠乏は、アレルギー性疾患や炎症性疾患の一因として関係していると言われています。191-193実際、食物反応と密接に関連する症状である湿疹や喘息の患者は、健康な個人よりも亜鉛の状態が低いことが一貫してわかっています。194,195これは、亜鉛が T 細胞集団に与える影響に一部起因している可能性があります。実験室での研究では、亜鉛のシグナル伝達は制御性 T 細胞と T ヘルパー 1 (Th1) 細胞を促進し、亜鉛欠乏は T ヘルパー 2 (Th2) 細胞の活動を増加させることで免疫応答を歪めることが示されています。191,193 アレルギー症状では、IgE を介した食物アレルギーを含む過剰な Th2 活性が見られます。7,196亜鉛の補給は、Th1/Th2 バランスの回復に役立つ可能性があります。191
さまざまな亜鉛トランスポーターが、メタロチオネインと呼ばれる亜鉛結合分子と連携して、亜鉛の吸収、細胞内外への移動、細胞内での分布を制御し、亜鉛の恒常性を制御し、免疫活動のバランスを維持します。192,197炎症と感染は、亜鉛トランスポーターの発現を変化させることで亜鉛の恒常性を乱すことが示されています。亜鉛欠乏は炎症の制御不良とアレルギー反応の増加を引き起こす可能性があるため、亜鉛枯渇とアレルギー/炎症の悪循環がある可能性があることを示唆しています。191
亜鉛の補給は腸壁の免疫機能のバランスを回復させる可能性があり、臨床研究では腸の炎症を軽減し、炎症性腸疾患の患者の健康を改善することが示されています。198一部 の前臨床および臨床証拠は、亜鉛補給が腸内壁の細胞間のタイトジャンクションをサポートすることで腸のバリア機能を改善する可能性があることを示唆しています。199-201腸の漏れを軽減することで、亜鉛 補給は食品に対する免疫反応を制限する可能性があります。動物実験では、亜鉛欠乏により腸の免疫寛容が抑制され、202亜鉛状態が低いと食品反応の可能性が高まる可能性がある別のメカニズムが実証されました。
ビーガン 食では亜鉛が不足することが多い。201亜鉛の吸収はクエン酸と食物タンパク質、特に動物性タンパク質によって促進される。一方、カルシウムとフィチン酸(植物繊維に含まれる)は亜鉛の吸収を阻害する。193,197発酵と発芽はフィチン酸を減らすことで食物中の亜鉛の利用性を高めることができる。197亜鉛塩(グルコン酸亜鉛、クエン酸亜鉛、酢酸亜鉛など)に比べて、酸化亜鉛は亜鉛濃度を高める効果が低いことが分かっているが、亜鉛塩は生物学的利用能に大きな変化がないようだ。197,203重要 なのは、PPI が正常な亜鉛吸収を阻害し、特定の利尿薬や降圧薬が亜鉛を枯渇させる可能性があることである。197,201
長期間にわたり1日あたり50mg以上の亜鉛を補給すると、銅と鉄の代謝が阻害され、亜鉛中毒やそれに関連する免疫機能障害を引き起こす可能性があることに注意することが重要です。症状には、吐き気、嘔吐、下痢、筋肉のけいれんなどがあります。197
プロピオニル-L-カルニチン
研究によると、 L-カルニチンの誘導体であるプロピオニル-L-カルニチン(PLC)は、潰瘍性大腸炎における腸の微小血管の修復と粘膜の炎症の軽減に役立つことが示唆されています。204 多施設共同第 2 相試験では、軽度から中等度の潰瘍性大腸炎の患者に、1 日 1 グラムの PLC、1 日 2 グラムの PLC、またはプラセボが投与され、PLC が症状の重症度に与える影響を評価しました。各試験参加者は、安定した経口薬も服用していました。結果によると、1 日 1 グラムまたは 2 グラムの PLC を服用した人の 72%(79 人中 57 人)は、プラセボを服用した人と比較して顕著な臨床反応を示し、1 日 1 グラムを服用した参加者で最も高い反応が見られました。205さらに、1 グラム群の参加者の 55%(40 人中 22 人)が寛解を経験しました。これらの結果は、PLC が軽度から中等度の潰瘍性大腸炎に対する有益な補助治療であることを示しています。食物反応および関連症状の改善における PLC の役割はまだ研究されていませんが、これは調査すべき研究分野であると思われます。
ビタミンD
ビタミンDは免疫機能と抗炎症経路の調節に重要な役割を果たしており、研究では、血中のビタミンDレベルの上昇が免疫反応の強化と炎症性サイトカインの産生の減少に関連していることが示されています。206,207さらに、日光への曝露によって生成されるビタミンDは、抗菌タンパク質を活性化し、腸内細菌叢を保護し、腸内バリア機能を強化し、肥満細胞、樹状細胞、T細胞の活動のバランスをとります。208
炎症性腸疾患の患者ではビタミン D の不足が免疫介在性炎症プロセスと関連しており、これらの疾患の患者ではビタミン D の値が通常より低いことが一般的です。207 ビタミンD の補給は腸疾患 (炎症性腸疾患など) の患者の健康状態の 改善に役立つ可能性がありますが、食物アレルギーや過敏症の患者に対する補給の効果はまだ解明されていません。しかし、この分野での研究は必要です。207,208
6食物反応の医学的治療
食物アレルギーは、重篤で生命を脅かす可能性のある合併症を引き起こす可能性があります。23,209食物に対するアレルギー反応が出ていると思われる場合は、すぐに医師の診察を受けてください。
食物反応の治療に使用できる薬にはいくつかの種類があります。23ただし、食品過敏症、アレルギー、不耐症の管理に適応外薬を使用する場合は、資格のある医療専門家の指導の下でのみ行う必要があります。210さらに 、症状の管理には薬に頼るのではなく、過敏症やアレルギーの根本的な原因に対処することが重要です。
注意:セリアック病の患者は、Life Extension のセリアック病および非セリアック性グルテン過敏症に関するプロトコルを参照してください 。
食物アレルギーの治療
食物アレルギーの治療では、原因となる食品を避けるのが主な戦略ですが、原因となる食品を摂取した場合に食物アレルギーの症状を軽減するのに役立つ、承認済みおよび適応外の治療法がいくつかあります。38真の食物アレルギーを持つ人は、自分にとって最適な治療法について、常に資格のあるアレルギー専門医に相談する必要があります。
エピネフリン。エピペン自動注射器は、食物アレルギーによるアナフィラキシーの緊急治療として、ホルモンおよび神経伝達物質であるエピネフリン(アドレナリン)を投与します。38 アナフィラキシーを経験したことがある人、またはアナフィラキシーのリスクがある人は、食物アレルゲンに対する体のアレルギー反応を急速に軽減するために、常にエピペンを携帯する必要があります。
適応外の抗 IgE 抗体。食物アレルギーの治療に適応外で使用されることがある 2 つの抗 IgE モノクローナル抗体は、オマリズマブ (ゾレア) とデュピルマブ (デュピクセント) です。22,211,212
経口免疫療法。ピーナッツ(Arachis hypogaea)アレルゲン粉末(Palforzia)は、ピーナッツアレルギーのある4~17歳の小児のアナフィラキシーを予防するために、最近FDAに承認された経口免疫療法薬です。213,214重要なのは、治療を受けている人は食事からピーナッツを厳重に避けなければならないということです。この薬は、偶発的な曝露による重篤な反応を防ぐことを目的としています。経口免疫療法については、「新しい治療法」のセクションでさらに詳しく説明します。
抗ヒスタミン薬とコルチコステロイド。ジフェンヒドラミン(ベナドリル)やセチリジン(ジルテック)などの抗ヒスタミン薬やプレドニゾンなどのコルチコステロイドを含むこれらのよく知られた薬は、食物アレルギーによって引き起こされる炎症反応の治療に使用されることがあります。215,216抗 ヒスタミン薬は一般に軽度のアレルギー反応に使用され、コルチコステロイドは一般に短期間使用され、その後、重度のアレルギー反応後の炎症を軽減するために徐々に減量されます。
アレルゲン免疫療法。アレルゲン免疫療法では、アレルギーのある人に数か月から数年かけて徐々にアレルゲンの量を増やして投与します。アレルゲン免疫療法の目的は、徐々に耐性をつけていき、アレルゲンに対する個人の免疫系を脱感作させることです。症状を軽減するのに役立つかもしれませんが、アレルゲン免疫療法では耐性を維持するためにアレルゲンに継続的にさらされる必要があります。このような治療法は、治療中に重度のアレルギー反応が起こる可能性があるため、通常は専門のクリニックで厳重な医師の監督の下でのみ提供されます。38
- 経口免疫療法。経口免疫療法では、通常、医師の厳重な監督下でアレルゲン抽出物を毎日経口投与します。一部の研究では、経口免疫療法はピーナッツ、牛乳、卵などの特定の食物アレルゲンに対する脱感作に効果的ですが、治療中に重度のアレルギー反応が起こるリスクがあり、脱感作を維持するためには治療を無期限に継続する必要がある可能性が高いことが示されています。217,218経口免疫療法薬の 1 つである Palforzia は、ピーナッツに対する重度のアレルギー反応のリスクを軽減することが FDA によって承認されています (上記を参照) 。219
- 皮膚免疫療法。皮膚免疫療法 (EPIT) では、アレルゲン抽出物を皮膚に貼付したパッチを通して投与します。この比較的新しい治療法は、現在、ピーナッツアレルギーの治療薬として評価されています。218,220 EPITはピーナッツに対する脱感作に効果があるようですが、脱感作を維持するには長期間にわたって治療を続ける必要があります。220,221
- 舌下免疫療法。舌下免疫療法 (SLIT) では、舌の下にアレルゲン抽出物を点眼薬または錠剤の形で徐々に投与します。この療法は、花粉症などの呼吸器アレルギーの治療に何十年も使用されており、食物アレルギーの治療にも研究されています。SLIT は、特定の食物アレルゲンに対する個人の感受性を低下させるのに効果的です。SLIT は通常、自宅で実施され、他の免疫療法よりも安全で便利であると考えられています。218
食物不耐症の治療
有害反応を引き起こす食品や成分を避けることが、食物不耐症の主な治療法です。しかし、ほとんどの不耐症は特定の酵素の欠乏が原因であることから、食事に酵素サプリメントを加えるという別の一般的な治療法もあります。最もよく推奨される 2 つの酵素サプリメントは、それぞれ乳糖不耐症と蔗糖不耐症の治療に使用されるラクターゼとサクロシダーゼです。27,36医療専門家の推奨に従って、胃酸逆流症用の市販薬や胃腸症状用の下痢薬を使用することで、食物不耐症の特定の症状が緩和される人もいます。
好酸球性食道炎(EoE)/好酸球性疾患(EGID)の治療
最近の臨床的証拠によると、動物性ミルクのみを除去することは、EoE 患者にとって有益な出発点となる可能性がある。約 6 週間、動物性ミルクの 1 食品除去食 (1FED) を行った患者では、EoE 症状が著しく改善し、血中の好酸球 (免疫細胞) レベルが大幅に低下し、34% で症状の完全寛解 (組織学的寛解) がみられた。107 1FED に反応しなかった患者は、EoE 症状の改善または組織学的寛解の可能性を高めるために、6 食品除去食 (6FED、動物性ミルク、小麦、卵、大豆、魚介類、ピーナッツ、木の実を除去) に進むことができ、6FED に進んだ患者のうち 43% で完全寛解がみられた。
食生活の変更を勧めるだけでなく、症状を管理し、炎症を抑え、組織の損傷を軽減するために薬が処方されることもあります。EoE の治療によく使用される薬には、胃酸の逆流を抑える PPI や、食道の炎症を抑えるコルチコステロイドなどがあります。
2022年にEoEの治療薬としてFDAの承認を受けたデュピルマブは、好酸球関連炎症に関与する2つの免疫タンパク質であるインターロイキン(IL)-4とIL-13を標的とする抗体です。222デュピルマブは他のEGIDの治療にも潜在的に有効であると思われるため、この特定の薬剤は非EoE EGIDに対するアプローチとして有望である可能性があります。
極端な場合には、食道や腸の狭窄部を広げるために内視鏡による拡張術が必要になることがある。223
7新たな治療法
ヒスタミン不耐症の治療
ヒスタミン不耐症は多くの医療提供者によってまだ医学的疾患として認識されていないため、ヒスタミン不耐症の治療に特に承認されている薬剤はありません。ただし、ヒスタミン不耐症に関連する症状の管理を助けるために、適応外で使用される薬剤もあります。
- ロラタジン(クラリチン)、フェキソフェナジン(アレグラ)、セチリジンなどの鎮静効果の少ない第 2 世代抗ヒスタミン薬は、アレルギー反応の治療によく使用され、かゆみ、じんましん、鼻水などのヒスタミン不耐症の症状の緩和にも役立ちます。ただし、消化器系の問題など、ヒスタミン不耐症に関連するすべての症状に効果があるわけではありません。23
- 過剰な免疫反応を抑制するコルチコステロイドも、ヒスタミン不耐症の症状の治療に有効である可能性があります。ただし、コルチコステロイドの大量使用は、時間の経過とともに免疫系を抑制する可能性があるため、これらの薬剤は一般に急性炎症発作に対して短期的に使用されます。低用量(たとえば、プレドニゾン 1 日 5 mg)は、長期使用に適しており、一般に重大な副作用を引き起こしません。23,224
- さらに、ヒスタミン不耐症の人の中には、クロモグリク酸ナトリウムやケトチフェンなど、肥満細胞を安定させる薬が有効な人もいます。8これらの薬は、肥満細胞からのヒスタミンやその他の炎症性化合物の放出を防ぐのに役立ち、じんましん、かゆみ、胃腸の不快感などの症状を軽減します。
ヒスタミン不耐症の患者の場合、薬物療法を主な治療方法として頼るべきではありません。最も効果的なアプローチは、通常、原因となる食品を特定し、食事から排除することです。医療従事者または登録栄養士と協力して適切な栄養を摂取し、関連する症状や状態を管理することも重要なアプローチです。
アレルギー
アレルギーに対する新しい治療法は、アレルゲンに対する免疫システムの過剰な反応を軽減することに重点を置いています。現在、新しい治療法の結果はさまざまですが、それぞれの治療法は脱感作の基本原則に重点を置いています。210
抗 IgE 戦略。抗 IgE 抗体はもともと喘息や慢性特発性蕁麻疹の治療薬として承認されていましたが、適応外使用で食物アレルギーの治療薬として使用されることもあります。225これらの抗体はすべての IgE 分子に結合するため、 1 つのアレルゲンまたは誘因に特異的ではありません。抗 IgE 抗体は、経口免疫療法などの免疫療法の前治療薬として使用して、アレルゲンに対する脱感作を促進することができます。220オマリズマブは、単独療法としても経口免疫療法との併用でも食物アレルギーの治療に有望な抗 IgE 抗体の 1 つです。226 リゲリズマブは、 2023 年後半現在、ピーナッツアレルギーの治療薬として第 3 相臨床試験が行われている別の抗 IgE 抗体です。227
食物アレルギー治療における IgE 関連のもう 1 つの戦略は、IgE 生成につながる免疫反応を防ぐことです。デュピルマブは、IL-4 受容体と呼ばれる特殊な構造に結合する抗体です。免疫タンパク質がアレルゲンに反応してこの受容体に結合すると、IgE の生成が増加し始めます。デュピルマブはこの相互作用を阻害し、免疫タンパク質が IL-4 受容体に結合するのをブロックすることで IgE の生成を防ぎます。デュピルマブは喘息やアトピー性皮膚炎などのいくつかの疾患の治療に承認されており、食物アレルギーの治療に有効かどうかを判断するための臨床試験がいくつか進行中です。22,212
好酸球性食道炎(EoE)と好酸球性疾患(EGID)
EoE や EGID などの複雑なアレルギー疾患は治療が難しい場合がありますが、いくつかの新しい治療法が研究されています。
抗体治療。2023年半ば現在、好酸球性疾患、特に EoE の治療を目的とした、次のような抗体が開発されています。
- リレンテリマブ。リレンテリマブ (AK002) は、好酸球と肥満細胞の表面に発現し、好塩基球では発現が低いタンパク質である、シアリン酸結合免疫グロブリン様レクチン (Siglec)-8 受容体を標的とする抗体です。Siglec-8 は、好酸球、肥満細胞、好塩基球に、感染症と戦うためにもはや必要ないことを伝える重要な免疫タンパク質です。免疫細胞 (好酸球、肥満細胞、好塩基球など) の過剰な活動は、アレルギー反応や過剰な免疫応答と関連しています。リレンテリマブは、第 2 相臨床試験で、好酸球によって引き起こされる炎症を軽減し、EoE の症状を改善する有望な結果を示しました。228リレンテリマブは、好酸球性胃炎、好酸球性十二指腸炎、好酸球性食道炎の希少疾病用医薬品として指定されています。229
- RPC4046。RPC4046は、第 2 相臨床試験で評価された IL-13 抗体です。この試験の結果、RPC4046 治療により、ステロイド抵抗性 EoE 患者の好酸球数が減少し、症状が改善することがわかりました。230,231この試験の非盲検延長試験では、RPC4046 による治療を最長 1 年間継続しても忍容性が高く、ベースラインと比較して EoE 疾患の内視鏡的、組織学的、臨床的指標が継続的に改善および/または維持されることがわかりました。232
- レスリズマブ。レスリズマブ(Cinqair)は、好酸球性喘息の治療薬として承認されている抗IL-5抗体です。233これまでのところ、EoEの結果は中程度の効果しか示していません。234
- ベンラリズマブ。ベンラリズマブ(ファセンラ)は、IL-5Rα受容体を阻害し、好酸球の活動と生存に関与するIL-5経路234,235を阻害することで喘息の治療に使用される抗体です。この経路を阻害すると、IgEの産生を減らすことができます。2023年後半現在、ベンラリズマブはEoEおよび好酸球性胃炎および胃腸炎の治療における有効性を調査するための第3相試験が行われています。234
- デュピルマブ。デュピルマブは IL-4 と IL-13 を標的とする抗体で、EoE、喘息、アトピー性皮膚炎、鼻茸を伴う慢性副鼻腔炎での使用がすでに承認されています。現在、他の好酸球性疾患についても評価中です。
- センダキマブ。センダキマブ(CC-93538)は、EoEの治療薬として臨床試験が行われている抗IL-13抗体です。236 2024 年初頭現在、進行中の後期段階(第3相)試験では、好酸球性食道炎の成人および青年を対象に、CC-93538による48週間の治療の有効性を検討しています。この試験は2024年後半に完了すると予想されています。237
開発中の他の治療法
- エトラシモド。エトラシモド(ベルシピティ)は、白血球がリンパ節から出て炎症を引き起こすのを防ぐ選択的スフィンゴシン-1-リン酸(S1P)受容体モジュレーターです。当初は潰瘍性大腸炎の治療薬として開発され、2023年後半現在、EoEの治療にも有効かどうかを評価する第2相臨床試験が行われています。236,238
- IRL201104。IRL201104は、結核菌が産生する免疫調節タンパク質から得られるペプチド薬です。このペプチド薬は、免疫系が抗原を認識する方法を変え、(2024年半ばの時点で)EoEの第2相試験が行われ、有望な初期結果が得られました。239 FDAは、 2024年1月にIRL201104に希少疾病用医薬品の指定を与えました。240
8よくある質問
食物反応を調べる検査にはどのようなものがありますか?
医師が食物反応を正確に診断するのは難しい場合があります。特定のケースでは複数の検査方法が使用されることがあり、食物反応を完璧に診断できる検査はないため、診断には複数の検査が必要になることがよくあります。資格のある医療専門家は、特定の症状に適した検査が選択されるように支援できます。次のような方法があります。
- アレルギー専門医による皮膚プリックテストとアトピーパッチテスト
- アレルギー専門医による経口食物負荷試験(あまり一般的ではない)
- 排除と再導入
- 血清免疫グロブリンE(IgE)検査(アレルギー専門医が行うことが多い)
- 血清免疫グロブリンIgGおよびIgAは、革新的な統合医療の医師によって推奨される可能性がある。
- 水素呼気検査は、通常は消化器専門医が行います。
- 消化器専門医による内視鏡検査と生検
食物反応の原因は何ですか?
食物に対する反応は、アレルギー、過敏症、不耐性の いずれかです。食物アレルギーは、IgE 抗体または T 細胞炎症カスケードのいずれかによって、免疫系が食物または食物成分に対して誤って反応することで起こります。5,6一方、食物不耐性は免疫反応とは関係なく、むしろ異常または不完全な消化に関係しています。24
食物過敏症は、IgG 抗体や IgA 抗体、またはヒスタミンやサリチル酸塩などの化学物質に対する過敏症、あるいは「腸漏れ」や類似の症状などの他の要因と関連している場合があります。
食物反応を引き起こす一般的な食品は何ですか?
多くの食品が食物反応を引き起こす可能性がありますが、引き金となる食品は人によって異なります。どの食品が問題になる可能性があるかを判断する最善の方法は、資格のある臨床医の指導の下で検査を受けることです。ただし、以下の食品または食品成分は食物反応と関連することがよくあります73 :
- 乳製品(乳糖)
- 卵
- ピーナッツ
- 大豆
- 生の果物や野菜
- 小麦
- カフェイン
- フルクトース
食物反応は時間の経過とともに発症する可能性がありますか?
はい、食物アレルギーは時間の経過とともに発症する可能性があり、以前はアレルギー反応がなかった食物が問題になることがあります。食物アレルギーは通常、幼少期に初めて現れますが、成人期や老年期に初めて反応が起こることもあります。8
残念ながら、食物アレルギー反応が起こる正確な原因は特定が難しく、複雑です。予備調査では、環境化学物質の中には、体内のタンパク質に結合する小さな分子であるハプテンとして作用するものがあることが示唆されています。タンパク質に結合すると、ハプテンはその構造を変化させ、免疫系を混乱させ、異常な自己免疫反応や炎症反応を引き起こす可能性があります。また、環境化合物の経口曝露が増えると、食物タンパク質に対する経口耐性の発達が妨げられ、食物タンパク質アレルギーになりやすくなるとも考えられています。これらの仮説を検証するには研究が必要です。241,242
特定の食品または食品成分を摂取した後に不快な症状に気付き始めた場合、たとえ以前は問題がなかったとしても、資格のある医療提供者と食品過敏症または不耐性の検査について話し合うことをお勧めします。
食べ物に対する反応はいつか消えるのでしょうか?
場合によっては、食物反応は時間の経過とともに消えたり、問題が少なくなったりすることがあります。ただし、食物に対して重度の反応を起こしたことがある場合、長期間その食物を避けていた場合は、事前に医師に相談せずにその食物を再び摂取しないようにしてください。免疫介在性アレルギーは、非免疫介在性不耐症よりも時間の経過とともに解消される可能性が低くなります。
食べ物の反応を逆転させることはできますか?
食物アレルギー(免疫介在性)と食物不耐症(非免疫介在性)の両方に治療法があります。治療法の効果は人によって異なります。食物アレルギーはほとんどの場合回復しない可能性がありますが、食物不耐症は人によっては時間の経過とともに改善する場合があります。
Share this post
- Tags: アレルギー, アレルギーリサーチ, アレルギーリサーチグループ, アレルギーリサーチ社
